Was ist Krebs?
Krebs bezeichnet die unkontrollierte Vermehrung und das wuchernde Wachstum von Zellen in Form einer bösartigen Gewebeneubildung oder einem bösartigen Tumor. Bösartig meint, dass neben der Zellwucherung auch gesundes Nachbargewebe zerstört und Tochtergeschwülste gebildet werden.

Die Überlebenszeit von Krebs-Erkrankten hat sich dank neuer Erkenntnisse in der Molekularbiologie und daraus ableitenden Therapieformen erheblich verbessert. Trotzdem verbreiten Tumorerkrankungen nach wie vor einen ganz besonderen Schrecken und werden mit einer kriegerischen Metaphorik belegt: Der Krebs muss „besiegt“ oder „bekämpft“ werden. Und bei geheilten Patienten sprechen wir von „Überlebenden“.

Wie entsteht Krebs?
„Keine“ notierte der altägyptische Arzt Imhotep in seinen medizinischen Fallgeschichten. „Keine“ war Imhoteps Antwort auf die Frage, welche Therapie bei einer Krebserkrankung empfehlenswert sei. Der alte Ägypter war allerdings auch weit entfernt davon zu verstehen, was diese Krankheit eigentlich ausmacht.
©iStock / Jezperklauzen
Damit der Körper wachsen und sich Gewebe (wie die Haut) ständig erneuern können, müssen sich Zellen teilen, das nennt sich in der Fachsprache Mitose. Dabei können Fehler passieren. Das wissen wir seit der Forschung des Pathologen Rudolf Virchow im 19. Jahrhundert: Er fand heraus, dass Krebszellen nicht einfach neu entstehen oder durch Bakterien in den Körper gelangen. Krebs bildet sich aus ehemals gesunden Zellen, die erkranken und sich dadurch verändern. Neben äußeren, erbgutschädlichen Einflüssen wie Tabakrauch oder Viren, die für entzündliche Prozesse im Körper sorgen, spielt auch das Erbe unserer Gene eine Rolle bei der Veranlagung für Krebs. Wenn Zellen also entarten, kann sich neues Gewebe bilden, das nicht normal ist. Eine solche Geschwulst oder Schwellung ist überall im Körper möglich. Mediziner bezeichnen das abnormale Gewebewachstum als Tumor.

©iStock / fizkes
Was ist ein Tumor? Was ist ein Karzinom? Was sind Krebs-Eigenschaften?
Das Wort Tumor enthält keinerlei Bewertung, denn Tumoren können sowohl gutartig als auch bösartig sein. Ein Tumor im Bauch ist genauso ein Tumor wie ein Tumor im Kopf. In der Medizin bedeutet das Wort Tumor lediglich Schwellung oder Neubildung. Korrekterweise ist im Fachjargon entweder von einem gutartigen (benignen) oder einem bösartigen (malignen) Tumor die Rede. Korrekt ist übrigens der Plural Tumoren, obwohl sich umgangssprachlich Tumore durchgesetzt hat.
Ein Synonym für Tumor ist Geschwulst. Falsch ist dagegen der Begriff Geschwür. So wird ein tiefer Hautdefekt bezeichnet, der nicht durch eine Verletzung entstanden ist. Auch ein Ödem ist nie ein Tumor. Ödeme sind Gewebeschwellungen durch die Einlagerung von Flüssigkeit.
Ob Organe, Weichteile, Drüsen oder Knochen, in jedem Gewebe können sich sowohl gut- als auch bösartige Wucherungen bilden. Manchmal entsteht aus einer zunächst gutartigen Veränderung auch Krebs. Bekannt dafür sind Darmpolypen, die häufig eine Vorstufe von Darmkrebs sind.
Gutartige Tumoren und Krebstumoren unterscheiden sich in wesentlichen Punkten.

©iStock / Kateryna Kukota
Krebs: Gutartige oder benigne Tumoren
Ein gutartiger Tumor / Krebs dringt nicht in fremdes Gewebe ein, es kann fremdes Gewebes aber beim Wachsen verdrängen. Die Zellen eines gutartigen Tumors unterscheiden sich kaum von denen des Ursprunggewebes. Mediziner sprechen von „differenzierten Zellen“.
Viele der benignen Tumoren sind von einer Kapsel aus Bindegewebe umgeben, sie lassen sich dadurch gut herausoperieren. Gutartige Tumoren bilden auch keine Ableger (Metastasen) an anderen Stellen des Körpers. Ist der Tumor entfernt, wächst er normalerweise nicht von neuem. Nach der Operation ist keine weitere Tumor-Therapie nötig. Der Patient gilt als geheilt.
Ein gutartiger Tumor beeinträchtigt den Zustand des Betroffenen nicht generell, außer wenn er etwa auf Strukturen im Körper drückt und deren Funktion behindert.

©iStock / Design Cells
Krebs: Bösartige oder maligne Tumoren (Malignome)
Bösartige oder maligne Krebs-Tumoren (maligne Erkrankung) charakterisiert, dass sie das umliegende Gewebe durchdringen und zerstören. Ist malignes Gewebe nach außen abgeschlossen und das umliegende Gewebe noch nicht betroffen, spricht die Medizin von einem Carcinoma in situ (dt.: Krebs am Ursprungsort). Bleibt der Tumor am Ursprungsort, heißt es, der Krebs bleibt stumm (ruhende Krebszellen).
Krebszellen haben kaum Ähnlichkeit mit dem Gewebe, aus dem sie ursprünglich stammen. Das Ursprungsgewebe kann aber Einfluss darauf haben, wie schnell ein Tumor wächst. Darmkrebs zum Beispiel gilt als sehr langsam wachsende Krebsentität (Krebsart).
Allgemein beschreibt die Tumorverdopplungszeit (TVDZ), in welchem Zeitraum sich das Volumen eines Tumors verdoppelt. Für kleinzellige Bronchialkarzinome werden Verdopplungszeiten von 50 bis 100 Tagen angegeben, für die nicht-kleinzelligen Bronchialkarzinome wird angenommen, dass sie sich etwa alle 100 bis 300 Tage verdoppeln. Die TVDZ kann sich im Laufe der Krankheit auch verändern.
Die Tumorzellen verschmelzen mit dem Gewebe, da Krebs so gut wie nie verkapselt ist. Der Chirurg erwischt daher selten sämtliche Krebszellen, oder die OP zerstört sehr viel umliegendes Gewebe. Nach einer Operation sind fast immer spezielle Tumor-Therapien nötig, etwa eine Chemotherapie oder Bestrahlung. Krebszellen dringen in Blutgefäße ein, verteilen sich so im ganzen Körper und bilden Tochtergeschwülste, die berüchtigten Metastasen. Krebs neigt zu Rezidiven, das heißt, dass er nach zunächst erfolgreicher Behandlung zurückkehrt.
Der Allgemeinzustand des Patienten verschlechtert sich zunehmend, wenn Krebstumoren wachsen.

©iStock / Md Babul Hosen
Tumor-Definition: solide Tumoren
Bösartige Tumoren können sich in allen Körpergeweben entwickeln. Grundsätzlich wird hier zwischen den beiden Formen solide Tumoren und systemischen Krebserkrankungen unterschieden: Solide Tumoren setzen sich in einem Organ örtlich fest. Sie untergliedern sich wiederum in die Gruppen Blastome, Karzinome und Sarkome.
Blastome heißen auch embryonale Tumoren. Sie kommen bei Kindern und Jugendlichen vor und sind während der Entwicklung von Organen und Geweben im Mutterleib entstanden.
Karzinome sind häufige bösartige Tumoren. Sie entstehen in den Organen, oft in Drüsen. Für den antiken griechischen Arzt und Lehrer Hippokrates hatten die Tumoren seiner Patienten gerade in der Brust entfernte Ähnlichkeit mit Krebsbeinen – von der Art, wie sie sich ausbreiten, aber auch, weil Geschwülste im Vergleich zum umliegenden Gewebe relativ hart sind – und er gab damit der Krankheit den Namen: Karkinos – Krebs. Vier von fünf bösartigen Tumoren sind ein Karzinom. Dazu zählen zum Beispiel das Mammakarzinom (Brustkrebs), das Pankreaskarzinom (Bauchspeicheldrüsenkrebs), Lungenkrebs (Lungenkarzinom oder Bronchialkarzinom), Darmkrebs (Kolonkarzinom oder Rektumkarzinom) oder das Zervixkarzinom (Gebärmutterhalskrebs). Beim Hautkrebs unterscheidet man den weißen Hautkrebs (Basalzellkarzinom oder Plattenepithelkarzinom) vom bösartigen schwarzen Hautkrebs (Malignes Melanom).
Sarkome sind seltene bösartige Tumoren des Weichteilgewebes, das heißt, dass Bindegewebe, die Muskeln oder das Fettgewebe betroffen sind. Mediziner unterscheiden Knochentumoren (Osteosarkom) und Weichteilsarkome. Da Sarkome aggressiv wachsen und oft in die Blutgefäße eindringen, ist das Risikio groß, dass sich Metastasen bilden. Allerdings sind nur etwa ein Prozent der bösartigen Tumoren Sarkome.

©iStock / Md Ariful Islam
Systemische Krebserkrankungen
Im Gegensatz zu den soliden Tumoren, die sich zunächst auf ein Organ beschränken, sind systemische Krebsereignisse von Anfang an eine Erkrankung des ganzen Organismus wie das Blutsystem oder das Lymphsystem. Daher zählen der Blutkrebs (die Leukämie) und der Lymphdrüsenkrebs (die Lymphome) zu dieser Krebsform.

Krebsentitäten: Welche Krebsarten gibt es?
Mehr als 300 verschiedene Krebsarten und Tumore sind bekannt. Krebsgeschwulste sind nicht auf bestimmte Zelltypen angewiesen und können praktisch überall im Körper auftreten. Die mit Abstand häufigste Krebsentität bei Frauen ist Brustkrebs mit etwa 70.000 Neuerkrankungen pro Jahr. Männer erkranken am häufigsten an Prostatakrebs (ca. 65.000 Neuerkrankungen pro Jahr). Lungen- und Darmkrebs stehen bei beiden Geschlechtern auf den Plätzen 2 und 3.
Wie gut die Überlebenschancen sind, hängt oft davon ab, in welchem Stadium der Krebs entdeckt wird.
©iStock / Alexander Traksel
Krebs-Tote Deutschland
232.700 Frauen und 265.200 Männer erkranken in Deutschland jährlich an Krebs (gesamt 497.900, Stand 2018). 104.791 Frauen und 124.274 Männer starben daran (gesamt 229.065). Zahlen über alle anderen denkbaren Geschlechtsidentitäten werden nicht erfasst.
(Quelle: https://www.krebsdaten.de/Krebs/DE/Content/Krebsarten/Krebs_gesamt/krebs_gesamt_node.html;jsessionid=D1CA6F0AD2EF75ABE7425C17BA0480EE.internet072)

©iStock / funky-data
Die häufigsten Krebs-Arten bei Männern (Neuerkrankungen pro Jahr)
- Prostatakrebs 65.200 (10-Jahrestendenz: + 2,8 %)
- Lungenkrebs 35.290 (+ 3,9 %)
- Darmkrebs 33.920 (– 4 %)
- Harnblasenkrebs 13.500 (+ 4,8 %)
- Malignes Melanom der Haut 12.010 (+ 34,8 %)
- Non-Hodgkin-Lymphome 10.190 (+ 40,2 %)
- Pankreaskrebs 9.860 (+ 33,4 %)
- Krebs von Mundhöhle und Rachen 9.820 (+ 3,2 %)
- Nierenkrebs 9.350 (+ 4,4 %)
- Magenkrebs 9.200 (– 0,1 %)
- Leukämien 6.870 (+ 8,4 %)
- Speiseröhrenkrebs 5.710 (+ 19 %)
- Hodenkrebs 4.160 (+ 4,8 %)
- Kehlkopfkrebs 2.770 (– 23,3 %)
- Schilddrüsenkrebs 1.930 (+ 12,9 %)
- Morbus Hodgkin 1.440 (+ 24,1 %)
Krebserkrankungen Männer gesamt: 265.170
(Stand 2018, Quelle: Deutsche Krebsgesellschaft)

©iStock / funky-data
Die häufigsten Krebs-Arten bei Frauen (Neuerkrankungen pro Jahr)
- Brustkrebs 69.900 (10-Jahrestendenz: – 2,5 %)
- Darmkrebs 25.710 (– 14,4 %)
- Lungenkrebs 21.930 (+ 40,8 %)
- Malignes Melanom der Haut 10.880 (+ 22,4 %)
- Gebärmutterkörperkrebs 10.860 (– 3,7 %)
- Pankreaskrebs 9.160 (+ 21 %)
- Non-Hodgkin-Lymphome 8.280 (+ 28,8 %)
- Eierstock- und Eileiterkrebs 7.300 (– 6,3 %)
- Magenkrebs 5.560 (– 16,5 %)
- Nierenkrebs 5.480 (– 1,1 %)
- Leukämien 5.310 (+ 4,5 %)
- Harnblasenkrebs 4.770 (+ 5,8 %)
- Krebs von Mundhöhle und Rachen 4.490 (+ 28,7 %)
- Gebärmutterhalskrebs 4.320 (– 11,5 %)
- Schilddrüsenkrebs 4.270 (+ 2,6 %)
- Speiseröhrenkrebs 1.840 (+ 33,3 %)
- Morbus Hodgkin 1.100 (+ 19,6 %)
- Kehlkopfkrebs 540 (+ 5,5 %)
Krebserkrankungen Frauen gesamt: 232.720
(Stand 2018, Quelle: Deutsche Krebsgesellschaft)

©iStock / Hiraman
Brustkrebs (Mammakarzinom)
Brustkrebs entsteht meist aus Zellen, die an der Funktion der Milchdrüsen beteiligt sind. Das Hormon Östrogen spielt dabei eine wichtige Rolle: Vor allem in der Pubertät und der Schwangerschaft regt es Stammzellen in den Milchdrüsen dazu an, sich massiv zu vermehren. Dieser natürliche Prozess kann eine fatale Wendung erfahren, wenn Genmutationen eine Reihe von Krebsgenen aktivieren: Die Zellen beginnen unkontrolliert zu wachsen und bilden Tumore.
Es sind vor allem zwei Arten von Zellen, die an der Entstehung von Brustkrebs beteiligt sind. In mehr als 80 Prozent der Fälle stammen die Tumoren von Epithelzellen ab, die das Innere der Milchgänge auskleiden. Das Wachstum dieser sogenannten duktalen Karzinome hängt oftmals stark von Hormonen ab. Seltener (in etwa 10 bis 15 % der Fälle) geht der Brustkrebs von Zellen der Drüsenläppchen aus. Diese Form wird lobuläres Karzinom genannt.
Rechtzeitig erkannt, sind die meisten Brustkrebserkrankungen heilbar. Die Zahl der Sterbefälle sinkt seit Jahrzehnten kontinuierlich, obwohl mehr Frauen an Brustkrebs erkranken. Fünf Jahre nach der Diagnose sind 87 Prozent der Patientinnen noch am Leben.
Bei etwa 71.000 Menschen in Deutschland wird pro Jahr Brustkrebs diagnostiziert. 99 Prozent davon sind Frauen. Nur 600 bis 700 Männer jährlich sind davon betroffen. Laut Statistik steigt das Brustkrebs-Risiko mit dem Alter und sinkt ab 75 Jahren wieder leicht ab.
Ein hohes Risiko tragen Frauen, bei denen Mutationen im BRCA1-Gen (Chromosom 17) oder im BRCA2-Gen (Chromosom 13) vorliegen. Kommen Brustkrebserkrankungen gehäuft in der Familie vor, sollte abgeklärt werden, ob Mutationen in diesen Genen vorliegen. Wird eine solche Mutation nachgewiesen, können eine engmaschige Überwachung und regelmäßige Kontrolle das Risiko minimieren. Allenfalls muss auch über eine vorsorgliche Operation gesprochen werden.
Laut Experten spielen Geschlechtshormone bei der Entstehung von Brustkrebs eine gewisse Rolle. So ist die Wahrscheinlichkeit, an Brustkrebs zu erkranken größer, je länger die Frau in ihrem Leben einen Zyklus hatte. Je früher die Monatsblutung und je später die Menopause eingesetzt ist, desto mehr steigt das Krebsrisiko. Schwangerschaften und Stillzeiten allerdings wirken sich positiv aus, da in diesen Perioden der Zyklus unterbrochen ist. Die Einnahme der Anti-Baby-Pille erhöht das Risiko eher geringfügig. Dagegen belegen Studien, dass bei einer Hormonersatztherapie (HRT) in den Wechseljahren das Erkrankungsrisiko tatsächlich mit der Zahl der Jahre steigt, in denen eine Frau ihren Hormonmangel künstlich mit Medikamenten ausgeglichen hat.
Auch ein ungesunder Lebensstil mit zu wenig Bewegung und Übergewicht kann das Risiko steigern, an Brustkrebs zu erkranken. Übermäßiger Alkoholkonsum wirkt sich ebenfalls negativ aus. Rauchen und Passivrauchen kann zwar andere Krebsarten verursachen, doch kann es nicht mit der Entstehung von Brustkrebs in Zusammenhang gebracht werden.
Die Behandlung bei Brustkrebs orientiert sich ganz stark an der Tumorbiologie. Dadurch ist eine Operation nicht mehr zwingend der erste Schritt. Oft kann davor mit einer medikamentösen Behandlung begonnen werden, wodurch sich schon Erfolge erzielen lassen. Chemotherapie und Bestrahlung zählen nach wie vor zu den wichtigsten Säulen der Behandlung. Aber auch andere Therapiemöglichkeiten stehen zur Verfügung. So werden bei hormonempfindlichen Formen von Brustkrebs Antihormone eingesetzt, welche die wachstumsfördernde Wirkung der Sexualhormone unterbinden. Neu ist außerdem die Immuntherapie. Sie verhindert, dass sich Tumorzellen vor dem eigenen Immunsystem verstecken können.
Die hoffnungsvollste Nachricht kommt aus den USA. Dort läuft eine Studie, in der Betroffene mit einem Impfstoff behandelt werden. Er wurde speziell gegen das dreifach negative Mammakarzinom entwickelt: Eine besonders aggressive Form, an der 12 bis 15 Prozent aller erkrankten Frauen leiden und die in den meisten Fällen tödlich endet.
Ihren Namen hat die Krebsform, weil den Tumorzellen drei bestimmte Proteine fehlen, die eigentlich auf Brustkrebs-Zellen vorhanden sind. Bereits vor Jahren wurde festgestellt, dass ein Eiweiß besonders häufig bei dreifach negativen Karzinomen vorkommt: das sogenannte α-Lactalbumin. Auch in gesundem Brustgewebe ist es zu finden, aber nur in der Schwangerschaft und Stillzeit. Die Impfung soll nun das Immunsystem dazu bringen, Zellen mit diesem Eiweiß zu entdecken und zu zerstören. Im Gegensatz zu Chemo- oder Strahlentherapie wird das umliegende Gewebe nicht geschädigt – was von großem Vorteil ist.
Nun hängt alles davon ab, ob die Frauen den Stoff gut vertragen und ob vor allem der Tumor bekämpft wird. Ergebnisse der Studie werden im Herbst 2022 erwartet.

©iStock / Mohammed Haneefa Nizamudeen
Lungenkrebs (Bronchialkarzinom)
Die unkontrollierte Vermehrung der Zellen und damit das Entstehen bösartiger Tumore geht meist aus den unteren Atemwegen (Bronchien) hervor. Das Heimtückische: Im weichen, dehnungsfähigen Gewebe des Atmungsorgans kann sich ein Karzinom lange Zeit ungestört ausbreiten, bis die Betroffenen merken, dass etwas nicht stimmt. Ärzte entdecken ihn oft nur zufällig, zum Beispiel wenn die Lunge geröntgt wird. Spätere Anzeichen für Krebs sind Schmerzen im Brustkorb oder eine chronische Bronchitis.
Die Form des Lungenkrebses und das Stadium der Krankheit bestimmen die Weiterentwicklung und die Therapie der Krankheit. Kleinzellige und nicht-kleinzellige Lungenkarzinome sind deutlich verschieden in ihrer feingeweblichen Struktur sowie im Wachstums- und Ausbreitungsverhalten.
Die nicht-kleinzelligen Lungenkarzinome (NSCLC) entwickeln sich langsamer und metastasieren später. Laut Krebsgesellschaft leben fünf Jahre nach der Diagnose nur mehr 21 Prozent der weiblichen und 16 Prozent der männlichen Patienten.
Besonders düster sind die Aussichten beim schnell wachsenden, kleinzelligen Bronchialkarzinom (SCLC). Es wandert rasch mittels Blutweg und Lymphbahnen in Lymphknoten, Lunge, Skelett, Knochenmark, Leber und Gehirn. Rund 15 Prozent der Lungenkrebspatienten sind von dieser aggressiven Form betroffen. Ihre 5-Jahres-Überlebensrate liegt bei unter 10 Prozent.
In Deutschland erkranken jährlich rund 57.000 Menschen an Lungenkrebs. Er ist damit die dritthäufigste Krebsart.
Rauchen ist zwar Risikofaktor Nummer 1, doch circa 12 Prozent der Betroffenen haben nie Zigaretten konsumiert. Bei ihnen scheinen Passivrauchen und Schadstoffe am Arbeitsplatz wie Asbest laut Experten Auslöser zu sein.
Ein weiterer Faktor ist das Lebensalter. Männer erkranken im Schnitt mit 70 Jahren an Lungenkrebs, Frauen mit 69 Jahren. Das Alter ist auch für die Behandlung von Bedeutung. Wenn man zusätzlich zum Lungenkrebs noch an anderen Erkrankungen leidet, können die Behandlungsmöglichkeiten eingeschränkt sein.
Wie bei jedem Karzinom ist die Chance auf Heilung bei einer frühen Diagnose am höchsten. Ist der Tumor noch klein, kann bestrahlt oder operiert werden. Gibt es schon Metastasen, erfolgt meist eine Chemotherapie, häufig in Kombination mit einer Immuntherapie.
Krebs-Forschung: Neue Studienergebnisse zu Lungenkrebs
Wissenschafts- / Medizinjournalistin

Dr. rer. nat. Miriam Sonnet
Wirkstoff Sotorasib gegen KRASG12C-Mutation
Die Gabe von zielgerichteten Substanzen ist eine relativ neue Strategie, um Krebserkrankungen zu behandeln. Zielgerichtete Medikamente kommen unter anderem bei Patienten mit nicht-kleinzelligem Lungenkrebs zum Einsatz. Im Januar 2022 wurde ein neuer Wirkstoff zugelassen: Sotorasib richtet sich spezifisch gegen eine bestimmte Veränderung in Lungenkrebszellen, die KRASG12C-Mutation. Diese tritt bei etwa 13 % aller Betroffenen mit nicht-kleinzelligen Lungentumoren auf. Die Zulassung basiert auf den Daten der CodeBreaK100-Studie. Mittlerweile stehen auch neuere Ergebnisse zur Wirksamkeit und Sicherheit des Medikaments zur Verfügung.
Jährlich erkranken in Deutschland circa 57.500 Menschen an Lungenkrebs.[1] Experten unterscheiden dabei zwischen „kleinzelligen“ und „nicht-kleinzelleigen“ Tumoren – je nachdem wie die Krebszellen unter dem Mikroskop aussehen.[2] Zur Behandlung kommen, je nach Situation des Patienten und den Eigenschaften des Tumors, Operation, Chemotherapie, Bestrahlung sowie zielgerichtete und immuntherapeutische Strategien infrage.[3]
Zielgerichtete Konzepte zählen zu den neueren Ansätzen. Diese wirken, wie der Name bereits vermuten lässt, ganz gezielt auf die Krebszellen: zum Beispiel auf Veränderungen im Erbgut, die ihr Zellwachstum antreiben. Die Erbgut-Veränderungen führen dazu, dass die Tumoren bestimmte Strukturen auf ihrer Oberfläche ausbilden, welche die zielgerichteten Medikamente angreifen können. Daher sollten Betroffene vor einer Therapie auf diese Veränderungen hin untersucht werden.[4] Vor allem beim nicht-kleinzelligen Lungenkrebs kommen zielgerichtete Substanzen zum Einsatz.
Mittlerweile existieren einige zielgerichtete Behandlungen, die sich gegen verschiedene Veränderungen der Krebszellen richten. Aber nicht alle dieser Mutationen sind tatsächlich angreifbar: Bisher galten zum Beispiel Veränderungen im KRAS-Gen als nicht adressierbar. Das änderte sich kürzlich durch die Zulassung von Sotorasib für die Therapie des nicht-kleinzelligen Lungenkarzinoms. Das Medikament richtet sich gezielt gegen eine bestimmte KRAS-Veränderung: die KRASG12C-Mutation. Sie ist in etwa 13 % der nicht-kleinzelligen Lungenkarzinome zu finden. Auch 1–3 % aller Darmkrebs-Patienten tragen eine solche Mutation. Grundlage für die Zulassung waren die Daten der CodeBreaK100-Studie.[5] Mittlerweile gibt es neuere Daten, welche die Wirksamkeit belegen.[6]
Studiendesign: Ziel der CodeBreak100-Studie war es, unter anderem Sicherheit und Effektivität von Sotorasib bei Personen mit verschiedenen Krebserkrankungen, welche die Mutation KRASG12C tragen, zu prüfen. Die Betroffenen erhielten das Medikament oral einmal täglich in verschiedenen Dosierungen.
Teilnehmer: Die 129 Studienteilnehmer waren mindestens 18 Jahre alt. Das mediane Alter betrug 62 Jahre. 59 von ihnen litten unter einem nicht-kleinzelligen Lungenkarzinom, 42 unter Darmkrebs und 28 unter anderen Tumoren. Die meisten Patienten waren stark vorbehandelt, mit einem Median von drei vorangegangenen Therapien. 60,5 % der Betroffenen hatten bereits mehr als drei Behandlungen für ihre Krebserkrankung erhalten. Von den Personen mit nicht-kleinzelligem Lungenkarzinom waren 89,8 % Raucher oder ehemalige Raucher.
Die Studienautoren untersuchten zunächst die Sicherheit der Therapie. Kein Patient starb aufgrund von Nebenwirkungen, die durch die Gabe von Sotorasib entstanden. Fast alle Teilnehmer (96,9 %) entwickelten aber Nebenwirkungen. Am häufigsten traten Durchfall (29,5 %), Fatigue (23,3 %) und Übelkeit (20,9 %) auf. Schwerere Nebenwirkungen (Schweregrad mind. 3) erlitten 52,7 % der Patienten.
Info: Was ist Fatigue?[7]
Bei der Fatigue handelt es sich um eine extreme Müdigkeit und Erschöpfung. Häufig tritt sie in Verbindung mit einer Krebserkrankung auf, aber auch zum Beispiel Patienten mit Parkinson, Multipler Sklerose oder Rheuma können betroffen sein. Die Fatigue steht dabei oft nicht in direktem Zusammenhang mit einer körperlichen oder geistigen Anstrengung. Betroffene berichten häufig, dass sich die Ermüdung durch Ruhephasen kaum verbessert.
56,6 % der Betroffenen entwickelten Nebenwirkungen, die mit der Sotorasib-Therapie in Zusammenhang standen. Solche vom Schweregrad 3 umfassten unter anderem Veränderungen der Leberwerte, Durchfall, Blutarmut und Leberentzündungen.
Effektivität von Sotorasib beim nicht-kleinzelligen Lungenkrebs
32,2 % der 59 Patienten mit nicht-kleinzelligem Lungenkarzinom sprachen in der Studie auf die Behandlung mit Sotorasib an, das heißt dass sich die Tumormasse zu einem bestimmten Anteil verringerte. In 88,1 % der Fälle konnte der Tumor für median vier Monate kontrolliert werden – hier kam es weder zu einer Verbesserung noch zu einer Verschlechterung der Erkrankung. Zum Zeitpunkt der ersten Analyse nach sechs Wochen schrumpfte das Karzinom bei 71,2 % der Betroffenen. Median war die Therapie 10,9 Monate wirksam. Zum Zeitpunkt der Datenanalyse erhielten 23,7 % der Teilnehmer noch immer die Studienmedikation. Das mediane progressionsfreie Überleben, also die Zeit, in der die Erkrankung nicht voranschritt, betrug 6,3 Monate.
Effektivität von Sotorasib bei Personen mit Darmkrebs
7,1 % (3 von 42) der Darmkrebs-Patienten sprachen auf die Therapie an. Bei 66,7 % konnte der Tumor stabilisiert werden. Das mediane progressionsfreie Überleben betrug 4 Monate.
Das gegen KRASG12C gerichtete Medikament Sotorasib war in der CodeBreaK100-Studie wirksam. Im Rahmen der Therapie traten meist geringgradige Nebenwirkungen auf, die vor allem den Magen-Darm-Trakt und die Leber betrafen.
Die Wirksamkeit der Substanz sei vielversprechend, postulieren die Forscher: Auf die bisher verfügbaren Behandlungsstrategien sprechen zum Beispiel nur 9 % bis 18 % der nicht-kleinzelligen Lungenkrebs-Patienten in der zweiten oder dritten Therapielinie an.
Info: Was sind Therapielinien?
Ärzte unterscheiden im Zuge der Krebsbehandlung verschiedene Therapielinien, da mit der Zeit häufig verschiedene Medikamente eingesetzt werden. Die aufeinander folgenden Behandlungsphasen können sich über eine lange Zeit, meist über Monate oder auch Jahre hinweg, erstrecken. Als „Erstlinientherapie“ wird die erste Behandlung nach der Diagnose bezeichnet. Kehrt die Erkrankung zurück (Rezidiv), erhalten die Betroffenen eine Zweitlinientherapie. Ist auch diese nicht langfristig erfolgreich, kommt es zu weiteren Therapielinien – Dritt-, Viert-, Fünftlinientherapie und so weiter.[8]
Mittlerweile gibt es aktuellere Daten aus der CodeBreaK100-Studie, welche die Wirksamkeit von Sotorasib belegen.
Studiendesign: Die Patienten erhielten einmal täglich Sotorasib oral in einer Dosierung von 960 mg. Die Behandlung erfolgte so lange, bis die Erkrankung voranschritt oder bis die Betroffenen inakzeptable Nebenwirkungen entwickelten. Median erhielten die Teilnehmer die Studienmedikation für 5,5 Monate. 32,5 % wurden sogar mindestens neun Monate damit behandelt.
Teilnehmer: Die 126 Teilnehmer im medianen Alter von 63,5 Jahren litten unter einem lokal fortgeschrittenen oder metastasierten nicht-kleinzelligen Lungenkarzinom mit KRASG12C-Mutation. 92,9 % waren Raucher oder ehemalige Raucher. Alle Betroffenen hatten bereits eine oder mehrere Therapien hinter sich. Bei zwei Personen konnte die Wirksamkeit nicht untersucht werden, sodass für die Effektivitäts-Analyse die Daten von 124 Erkrankten zur Verfügung standen.
Ergebnis: 3,2 % der Patienten sprachen komplett auf die Therapie an, das heißt es war kein Tumor mehr nachweisbar. 33,9 % sprachen zumindest teilweise an. In 80,6 % der Fälle konnte die Erkrankung kontrolliert werden. Das mediane progressionsfreie Überleben betrug 6,8 Monate. Insgesamt lebten die Betroffenen median 12,5 Monate.
99,2 % der Teilnehmer entwickelten Nebenwirkungen. Auch hier waren am häufigsten Durchfall, Übelkeit, Fatigue und Leberwertveränderungen zu beobachten. Zudem traten Gelenkschmerzen häufiger auf. In 69,8 % der Fälle führten die Studienautoren die Nebenwirkungen auf die Sotorasib-Therapie zurück. 7,1 % der Patienten brachen die Behandlung aufgrund therapiebedingter Nebenwirkungen ab.
Fazit: Die Studienteilnehmer profitierten von der Sotorasib-Therapie. In einer neuen Studie – CodeBreaK200 – soll jetzt die Wirksamkeit von Sotorasib mit einem anderen Medikament bei Lungenkrebs-Erkrankten verglichen werden.
[1] https://www.krebsinformationsdienst.de/tumorarten/lungenkrebs/index.php (letzter Aufruf am 14.4.2022)
[2] https://www.krebsinformationsdienst.de/tumorarten/lungenkrebs/faq.php (letzter Aufruf am 14.4.2022)
[3] https://www.krebsinformationsdienst.de/tumorarten/lungenkrebs/behandlung-uebersicht.php (letzter Aufruf am 14.4.2022)
[4] https://www.krebsinformationsdienst.de/service/iblatt/iblatt-lungenkrebs-zielgerichtete-therapie.pdf?m=1649404045& (letzter Aufruf am 14.4.2022)
[5] Hong DS et al. N Engl J Med. 2020 Sep 24;383(13):1207-1217.
Skoulidis F et al. N Engl J Med. 2021 Jun 24;384(25):2371-2381.
[6] https://deutsche-fatigue-gesellschaft.de/fatigue/was-ist-fatigue/ (letzter Aufruf am 14.4.2022)
[7] https://www.krebs.de/krebstherapie/therapieoptionen-und-planung (letzter Aufruf am 14.4.2022)

©iStock / AND-ONE
Prostatakrebs
Prostatakrebs oder Krebs der Vorsteherdrüse entsteht zunächst im Inneren des männlichen Sexualorgans. Er kann aber das Bindegewebe der Kapsel durchdringen und dann Metastasen unter anderem in Samenblase, Harnblase und Mastdarm bilden. Im weiteren Verlauf der Krankheit können die Tumorzellen über das Lymphsystem und die Blutbahnen auch andere Körperteile wie Beckenknochen, Wirbelsäule, Rippen, Leber und Lunge befallen.
Prostatakrebs wächst sehr langsam. Deswegen haben betroffene Männer eine deutlich mehr als 90-prozentige Überlebenschance, wenn der Krebs erst jenseits des 70. Lebensjahres auftritt und nicht sehr aggressiv ist.
Mit etwa 65.000 neuen Fällen pro Jahr ist Prostatakrebs die häufigste Krebserkrankung bei Männern in Deutschland. Vor dem 50. Lebensjahr ist das Erkranken der Vorsteherdrüse, medizinisch Prostata, selten.
Eine gesunde Ernährung mit Gemüse, Obst, Fisch und Kräutern trägt zum Schutz der Vorsteherdrüse bei. Der Verzehr tierischer Produkte sollte stark reduziert werden. Bei einer US-Studie mit fast 77.000 Männern stellte sich heraus, dass starker Konsum von rotem Fleisch ein 2,5-fach erhöhtes Risiko für ein Prostatakarzinom bedeutet. Verantwortlich dafür könnte ein Stoff mit dem Namen Phenylacetylglutamin sein.
Generell hat jeder Mann ab 45 Jahren einmal im Jahr Anspruch auf ein Prostata-Screening. Hier kann Krebs in einem frühen Stadium entdeckt werden. Sollte er beim Vater, Bruder, Onkel oder Großvater in jungen Jahren aufgetreten sein, sind Früherkennungsuntersuchungen schon ab einem Alter von etwa 35 Jahren empfehlenswert.
Eine Veränderung der Prostata lässt sich durch Ultraschall oder mithilfe der Bestimmung eines prostataspezifischen Antigens (PSA) entdecken. Gewissheit bringt eine Biopsie, bei der eine Gewebeprobe entnommen wird. Wird ein Karzinom diagnostiziert, besteht nicht sofort Handlungsbedarf. Bleibt der Tumor auf die Vorsteherdrüse begrenzt, raten Ärzte, erst einmal abzuwarten.
Ist ein Eingriff nötig, erfolgt dieser heute minimal-invasiv. Über kleine Schnitte werden bei der radikalen Prostatektomie die Instrumente eingeführt und das entartete Gewebe wird entfernt. Mit 2.600 Patienten pro Jahr weltweit führend bei diesem Eingriff ist die Hamburger Martiniklinik, eine Tochtergesellschaft des Universitätsklinikum Eppendorf (UKE), die ausschließlich Prostatapatienten behandelt.
Alternativ zur OP kann eine Bestrahlung erfolgen. Hier wird die Prostata über mehrere Wochen von außen behandelt. Eine Methode von innen ist die Brachytherapie. Hier werden mithilfe einer Sonde winzige radioaktive Metallstäbe in die Vorsteherdrüse gebracht. Ziel beider Verfahren ist es, Krebszellen zu zerstören (medizinisch: abladieren).
Neu und mit deutlich weniger Nebenwirkungen (Impotenz, Inkontinenz) ist eine Irreversible Elektroporation (IRE), bei der mittels ultrakurzer Stromstöße die Krebszellen zerstört, Bindegewebe und Nerven aber erhalten bleiben. Weltweit führend bei diesem extrem schonenden Eingriff ist das Vitus Prostata Center in Offenbach.
Fast alle Männer überleben eine Erkrankung an Prostatakrebs, wird er so frühzeitig erkannt wird, dass er noch auf die Vorsteherdrüse beschränkt ist. Die Zahl der (diagnostizierten) neuen Prostatakrebsfälle nimmt seit mehreren Jahrzehnten zu, ohne dass die Sterblichkeit steigt. Die relative 5-Jahres-Überlebensrate hat sich mittlerweile auf etwa 93 Prozent erhöht.

©iStock / Benjamin Toth
Schwarzer Hautkrebs (Malignes Melanom) und heller Hautkrebs (Basalzellkarzinom, Plattenephithel-Karzinom)
Hautkrebs entsteht meistens durch die ultraviolette Strahlung (UV-Strahlung) der Sonne. Wie Zellen sich teilen und entwickeln, wird durch das Erbgut im Zellkern gesteuert. UV-Strahlung kann dieses Erbgut beschädigen. Dadurch können aus einzelnen Zellen Nachkommen entstehen, die nicht mehr aufhören, sich zu teilen – die Krebszellen. Das Abwehrsystem des Körpers bekämpft solche entarteten Zellen zwar sehr wirksam, doch manchmal schlüpft eben doch eine veränderte Zelle durch die Kontrolle, und es entstehen Krebsgeschwüre. Dabei muss zwischen zwei Arten unterschieden werden:
- Der helle Hautkrebs, zu dem das Basalzellkarzinom und das Plattenephithel-Karzinom zählen, ist deutlich verbreiteter als der schwarze Hautkrebs, bildet aber seltener Metastasen. Kennzeichen sind leichte Verhornungen oder schuppige Veränderungen auf der Haut, vornehmlich an Stellen, die besonders der Sonneneinstrahlung ausgesetzt sind wie Gesicht, Ohren, Hände oder Nacken.
- Das maligne Melanom, schwarzer Hautkrebs, ist die gefährlichste Form des Hautkrebses. An ihm sterben Betroffene in der Regel nicht, aber an den Metastasen, die sich rasch über das Lymphgefäßsystem oder die Blutbahn im Körper ausbreiten. 90 Prozent der Sterbefälle bei Hauttumoren gehen auf das Konto von schwarzem Hautkrebs – dabei ist er durchaus heilbar, wird er frühzeitig entdeckt. Aktuell liegen für Frauen mit malignem Melanom der Haut in Deutschland die relativen Fünf-Jahres-Überlebensraten bei 95 Prozent und für Männer bei 93 Prozent.
Hautkrebs gehört mit zu den häufigsten Tumorarten. Derzeit erkranken in Deutschland schätzungsweise jährlich mehr als 250.000 Menschen an hellem Hautkrebs und circa 23.000 an schwarzem Hautkrebs. Während der weiße Hautkrebs überwiegend im höheren Lebensalter auftritt, trifft der schwarze Hautkrebs auch viele jüngere Menschen. Das typische Erkrankungsalter bei Frauen liegt im Durchschnitt bei 60 Jahren, bei Männern bei 68 Jahren.
Der Zusammenhang zwischen UV-Strahlung aus der Sonne oder dem Solarium und Hautkrebs ist eindeutig nachgewiesen, da die Veränderungen im Erbgut der Hautkrebs-Zellen spezifisch für diese Strahlung sind. Besonders anfällig sind helle Hauttypen, insbesondere blonde und rothaarige und Menschen, die zu Sommersprossen neigen, schlecht bräunen oder zu Sonnenbränden tendieren. Auch Menschen mit einer hohen Anzahl an angeborenen Leberflecken, vor allem besonders große, tragen ein erhöhtes Risiko.
Schließlich können sich Medikamente, die das Immunsystem unterdrücken, oder eine Strahlentherapie ebenfalls begünstigend auf die Entstehung von Hautkrebs auswirken.
Je nach Hautkrebsart und Krebsausdehnung gibt es unterschiedliche Therapien. Tumore werden herausgeschnitten, manchmal auch bei minus 170 Grad vereist, mit Laserstrahlen vernichtet oder durch Aktivierung des körpereigenen Immunsystems zerstört. Bei letzterer Methode wird der Hauttumor eingecremt und mit Rotlicht bestrahlt.
Hautärzte raten zur Vorsorge durch ein Hautkrebs-Screening einmal im Jahr. Dabei sucht der Dermatologe die Haut des Patienten auf mögliche Veränderungen ab. Zudem sollte direkte Sonneneinstrahlung vermieden werden.
Forscher aus Norwegen und den USA haben bereits Untersuchungen an Menschen mit einer Impfung durchgeführt, wenngleich mit nur 20 Personen, was eine sehr kleine Anzahl ist. Hier haben Menschen mit einer bösartigen Hautkrebs-Form ein Vakzin (Impfstoff) namens UV1 bekommen. Mit beigemischt war noch der Antikörper Pembrolizumab. Laut den Wissenschaftlern sprachen 60 Prozent der Patienten auf die Wirkstoff-Kombination an. Die Überlebenszeit stieg von rund neun Monaten auf 18,9 Monate an. Bei sechs Personen war der Tumor sogar komplett verschwunden. Weitere Studien mit mehr Teilnehmern werden derzeit vorbereitet.

©iStock / mi-viri
Gebärmutterhalskrebs (Zervixkarzinom)
Gebärmutterhalskrebs wird von Humanen Papillomviren (HPV) ausgelöst. Bekannt sind etwa 100 HPV-Typen, die wir in unserem Körper tragen, ohne dass wir es merken. Die meisten bringen lediglich gutartige Hautveränderungen wie Warzen an den Händen oder auch im Genitalbereich hervor. Es gibt aber auch Viren, die Zellveränderungen verursachen. Auch das ist zunächst völlig normal. Die meisten Frauen und Männer infizieren sich im Laufe ihres Lebens mindestens einmal mit HPV. Im Normalfall werden die Erreger vom Immunsystem bekämpft. Passiert das aber nicht, kann es zu einer Krebsvorstufe und später zu einem Karzinom kommen.
Für die Diagnose des Gebärmutterhalskrebses gibt es zwei Methoden:
- Die erste Variante ist die sogenannte Zytologie, besser bekannt als Pap-Test. Hier nimmt der Gynäkologe einen Zellabstrich vom äußeren Muttermund und dem Gebärmutterhalskanal. Im Labor wird der Abstrich mikroskopisch auf krankhaft veränderte Zellen untersucht.
- Die zweite Möglichkeit ist der HPV-Test. Hier können die Frauenärzte die DNA des Virus nachweisen und herausfinden, ob eine Infektion vorliegt. Eine neue Methode ist die Dünnschichtzytologie, die beide Nachweismöglichkeiten miteinander kombiniert.
Laut Berufsverband der Frauenärzte in Deutschland (BVF) erkranken jährlich etwa 4.500 Frauen an Gebärmutterhalskrebs (Zervixkarzinom). Aber: Durch entsprechende Vorsorge kann die Gefahr, an dieser Krebsart zu erkranken, um mehr als 90 Prozent gesenkt werden.
Humane Papillomviren werden über den direkten Kontakt von Mensch zu Mensch übertragen. Das geschieht fast immer in den schönsten Stunden der körperlichen Liebe.
Etwas präziser wird das Robert-Koch-Institut: „Die Viren dringen über Mikroverletzungen der Haut bzw. Schleimhaut ein und infizieren die Epithelzellen der Basalzellschicht. Hauptübertragungswege bei Infektionen im Anogenitalbereich sind Vaginal- und Analverkehr. Über orogenitale Sexualpraktiken ist eine Transmission in die Mundhöhle oder den Oropharynx möglich. Ebenfalls ist eine Übertragung durch sehr engen Körperkontakt (trotz Kondomnutzung beim Geschlechtsverkehr) möglich.“
Diesem Infektionsweg kann laut RKI ein weiterer folgen: „Zudem ist selten eine Übertragung von der Mutter auf das Neugeborene während der Geburt möglich.“
Hinter diagnostizierten Auffälligkeiten stecken meist harmlose Veränderungen, die sich selbst zurückbilden oder mit einer Konisation (Gewebeentnahme am Muttermund) behandelt werden können. Im fortgeschrittenen Stadium ist eine umfangreiche Operation nötig. Dabei muss oftmals die Gebärmutter entfernt werden (Hysterektomie).

Diagnose Krebs: Wie geht’s weiter?
Wer sich Unterstützung sucht, kommt psychisch und physisch besser mit der Krebserkrankung zurecht. Anlaufstellen für Krebserkrankungen sind zum Beispiel Onkolotsen, Onkopsychologen, Selbsthilfegruppen und spezielle Programme für die Nachsorge.
©iStock / gorodenkoff
Der Tod scheint nach einer Krebs-Diagnose allgegenwärtig, der eigene Körper zerbrechlich. Gedanken und Gefühle fahren mit dieser Diagnose Achterbahn, trotzdem müssen Betroffene funktionieren und das ganze Leben neu organisieren. Sie brauchen Informationen über Behandlungsmöglichkeiten und Therapieformen. Viele sind traumatisiert, haben das Gefühl, von der Situation überwältigt zu werden und drohen, in ein emotionales Loch zu fallen. Um das zu verhindern, gibt es professionellen Beistand.
Im folgenden stellen wir Ihnen einige mögliche Anlaufstellen für Psyche und Physis vor, ohne Anspruch auf Vollständigkeit.

©iStock / mehmetbuma
Erste Anlaufstellen: Krebsklinik und Krebsberatungsstellen
Erste Anlaufstellen sind die Klinik während des stationären Aufenthalts oder ambulante Krebsberatungsstellen. Telefonische Beratung bietet das Infonetz Krebs. Weitere Ansprechpartner sind Tumorzentren und Sozialdienste. Allerdings informieren diese Adressen in erster Linie zur Rehabilitation, Schwerbehindertenrecht, sonstigen Leistungen der Sozialversicherungsträger, zur Berufstätigkeit und zu finanzieller Unterstützung.
Experten kritisieren, dass viele Krebspatienten gar nicht wissen, wohin sie sich mit ihren Fragen wenden könnten. Der Zugang zu Sozialberatungen, zum Beispiel durch flächendeckende Krebsberatungsstellen, müsse dringend verbessert werden. Auch bei der Kommunikation zwischen den einzelnen Leistungsträgern (Krankenkassen, Rentenversicherung und Arbeitsamt) gebe es Optimierungs-Potenzial.
Onkolotsen: Orientierung für Krebsberatung und Krebsbehandlung
Wertvollen Beistand leistet daher spezialisiertes Fachpersonal wie Onkolotsen oder Psychoonkologen. Sie helfen nicht nur, mit den Emotionen umzugehen, sondern helfen den Patienten auch, die Irrwege der Bürokratie zu meistern. Die „menschlichen Rettungsanker“ sind im Idealfall ab der Diagnosestellung über die stationäre Versorgung und die anschließende Therapie bis hin zur mehrjährigen Nachsorge für den an Krebs erkrankten Menschen da.
Onkolotsen haben die Zeit, den Patienten in Ruhe Behandlungsmöglichkeiten aufzuzeigen und gemeinsam mit ihnen Anträge auszufüllen. Sie weisen darauf hin, dass sie sich in Krebskompetenzzentren eine zweite oder auch dritte Meinung einholen können oder Anspruch auf eine Haushaltshilfe haben, wenn Kinder im Spiel sind.
Wichtig zu wissen: Onkolotsen sind keine Ärzte. Sie fällen keine Entscheidung, sie können nur Denkanstöße geben.
Auch der Austausch mit Angehörigen ist enorm wichtig, denn diese leiden ebenfalls oft stark unter der Situation. Viele haben eine Dreifachbelastung: die eigenen Kinder, den Beruf und den Erkrankten. Eine Aufgabe kann es auch sein, einen Angehörigen in den Arm zu nehmen, weil er vor Erschöpfung weint. Bisher gibt es Onkolotsen in acht Bundesländern, vor allem in Sachsen, Sachsen-Anhalt und Schleswig-Holstein. Teilweise arbeiten sie ehrenamtlich, teilweise kostenpflichtig.
Die Sächsische Krebsgesellschaft leitet das bisher einzige Ausbildungsangebot für Onkolotsen. Während der 18-monatigen Ausbildung werden neben dem Hintergrundwissen zum Krebs-Verlauf psychosoziale Lernhinhalte vermittelt. An der Fortbildung nehmen Personen teil, die bereits im Feld der Onkologie arbeiten: Krankenschwestern, Pfleger oder Apotheker. Die Krankenkassen übernehmen das Honorar bisher nur bei Pflegefällen ab dem Pflegegrad 1.

©iStock / Ridofranz
Psychoonkologen: Fachkräfte für die krebskranke Seele
Psychoonkologen dagegen haben in der Regel ein human- oder sozialwissenschaftliches Studium absolviert. Wer in dieser Funktion in einem Krebszentrum oder einer Uniklinik arbeiten will, muss eine von der Deutschen Krebsgesellschaft zertifizierte Weiterbildung nachweisen. Ein Psychoonkologe sollte in der Regel fit sein in den Bereichen Sozialberatung, Psychotherapie, Schulmedizin, Komplementärmedizin, Entspannungsverfahren, aber auch existenzielle Psychotherapie und Philosophie.
Zu seinen Aufgaben gehört es vor allem, Hürden in der Kommunikation, auch Sprachlosigkeit, zwischen dem Patienten und seinem Umfeld zu überwinden. Umfeld umfasst hierbei nicht nur Angehörige, sondern vor allem auch Mediziner. Ärzte, die vielleicht nicht immer die perfekten Kommunikationsfähigkeiten mitbringen, treffen auf Patienten im Schockzustand … da kommt es leicht zu Missverständnissen und falschen Rückschlüssen.
Darüber hinaus erhalten Patienten von Psychoonkologen Unterstützung dabei, sich mit ihrer Diagnose auseinanderzusetzen. Dazu gehört unter anderem, wichtiges Hintergrundwissen aufzubauen. Denn ein informierter Patient, fühlt sich der Situation (und den Ärzten) weniger ausgeliefert und kann seiner Verzweiflung und Angst mit nüchternen Fakten entgegentreten, was die Lebensqualität insgesamt in dieser Situation verbessert.
Wer ein Deutschland eine psychoonkologische Betreuung benötigt, der erhält sie – egal ob gesetzlich oder privat versichert. Der behandelnde Arzt kann eine entsprechende Überweisung ausstellen.
Krebs-Selbsthilfegruppen: Offene Gespräche bei gleicher Perspektive
Eine gute Alternative bieten für manche Patienten auch Selbsthilfegruppen. Die Gemeinschaft aus Menschen, die gleiche oder ähnliche Erfahrungen gemacht haben, kann eine starke Energie freisetzen, wie viele Studien belegen. Die Verbundenheit stärkt, trägt, unterstützt, tröstet, motiviert: „Ich kann Dir nicht sagen, wie man es behandelt. Aber ich kann Dir sagen, wie es mir geholfen hat.“ So lernen die Teilnehmer in einem geschützten Rahmen von- und miteinander, vermitteln Wissen und stärken die eigene Gesundheitskompetenz. Da alles, was bei einem Meeting besprochen wird, in der Gruppe bleibt und nichts nach draußen dringt, haben die Mitglieder die Möglichkeit, sich zu öffnen.
Gesundheitsbezogene Selbsthilfegruppen können über die gesetzlichen Krankenkassen eine finanzielle Förderung erhalten. Auch Bürgerstiftungen und ähnliche Privatorganisationen bringen sich mit Spenden bei den selbst organisierten Gruppen ein.

©iStock / SDI Productions
Tumorzentren: Breast careness – Spezialprogramme beim Mammakarzinom
Tumorzentren, die auf Brustkrebs spezialisiert sind, haben häufig eigene Einrichtungen etwa zur „breast careness“ – spezielle Programme zur Nachsorge, außerdem sehr viele ehrenamtliche Hilfsangebote wie Selbsthilfegruppen oder Sorgentelefone.
Die oft freiwilligen Helfer leisten dort eine sehr wichtige Arbeit, geben den Frauen den Halt, den sie benötigen und der im medizinischen Alltag nicht immer möglich ist. Diese Hilfsangebote werden von Ärzten auch stets empfohlen, Infomaterialien werden Patientinnen zur Verfügung gestellt und sie werden ermutigt, solche Gruppen aufzusuchen.
Onkologische Reha-Zentren: Individuell betreut in den Alltag zurückfinden
In onkologischen Rehabilitationseinrichtungen ist es von besonderer Bedeutung, dass die verschiedenen medizinischen, physiotherapeutischen, psychologischen und kreativtherapeutischen Fachrichtungen gut koordiniert und aufeinander abgestimmt Hand in Hand arbeiten.
Die Therapie in der Reha-Klinik wird grundsätzlich am körperlichen und mentalen Zustand jedes einzelnen Patienten ausgerichtet. Es werden keine pauschalen, sondern individuelle Behandlungspläne ausgestellt und umgesetzt. Dabei besteht das ausdrückliche Ziel darin, dass der Patient nicht passiver Teilnehmer seines Reha-Programms bleibt, sondern erfolgreich dazu motiviert wird, den Aufenthalt in der Reha-Klinik aktiv mitzugestalten. In der Rehabilitation Krebskranker hat die psychosoziale Perspektive einen hohen Stellenwert ein. Denn schließlich soll der Betroffene mit der Reha-Maßnahme Mittel und Wege an die Hand bekommen, um sich nach der Reha wieder in ein Alltagsleben einzugliedern, in dem er selbst Verantwortung übernimmt.
Wird eine Reha-Maßnahme zur Wiederherstellung der Gesundheit verordnet, zahlt meist die Krankenkasse. Eine Maßnahme zur Wiederherstellung oder zum Erhalt der Erwerbsfähigkeit finanziert in der Regel der Rentenversicherungsträger.

©iStock / Stadtratte
Krebs-Nachsorge: Finanziell hilft der Härtefonds der Deutschen Krebshilfe
Nach der Reha folgt die Nachsorge, sie zählt zu den Leistungen der Deutschen Rentenversicherung. In dieser Phase geht es darum, den Erfolg der Krebstherapie zu beobachten, die Ergebnisse der Reha zu festigen, ein Auge auf mögliche Rückfälle zu haben und den Patienten für den Alltag stark zu machen, zum Beispiel ihn bei der sozialen und beruflichen Wiedereingliederung zu begleiten.
Je nach Krebsart ist ein anderer Nachsorge-Zeitraum vorgesehen. Manche Krebspatienten müssen nach überstandener Krankheit für den Rest ihres Lebens in die Nachbeobachtung. Betroffene berichten, dass es sehr belastend ist, sich immer und immer wieder Untersuchungen zu stellen und mit dem Thema Krebs auseinandersetzen zu müssen. Für manche Patienten ist deshalb zusätzlich eine psychologische Betreuung wichtig.
Die meisten Krebskrankheiten bringen Patienten an ihre finanzielle Grenze. Viele schämen sich für ihre Geldsorgen und möchten erst gar nicht darüber sprechen. Da ist es gut zu wissen, dass es einen Härtefonds der Deutschen Krebshilfe gibt. Er ist für finanziell in Not geratene Menschen gedacht, die nur ein niedriges Einkommen haben, wenig Krankengeld oder eine geringe Erwerbsminderungsrente bekommen. Die Zuwendung ist an Familien-Einkommens-Grenzen gebunden. Das monatliche Nettoeinkommen abzüglich der festen monatlichen Ausgaben durfte im Jahr 2019 folgende Grenzen nicht übersteigen:
- bei einer Person 424 Euro
- bei zwei Personen 725 Euro
- bei drei Personen 1074 Euro
Etwa 12.000 Anträge erreichen die Deutsche Krebshilfe jährlich. Allein 2019 unterstützte sie auf diesem Weg mehr als 7.400 Menschen mit 4,6 Millionen Euro. Es gibt in der Regel nur eine einmalige Geldleistung. Sie richtet sich nach der Bedürftigkeit und lag 2019 zwischen 440 Euro und 800 Euro. Die Gelder stammen aus Spenden an die Deutsche Krebshilfe.

Die wichtigsten Bausteine der modernen Krebs-Therapie
Sie teilen sich unkontrolliert, zapfen Blutgefäße an und wandern in benachbarte Gewebe: Bösartige Zellen, die sich in Organen, im Knochenmark oder in Lymphbahnen ausbreiten, sind die Ursache für eine der größten Gesundheits-Geiseln der Menschheit. Doch dank einer weiterentwickelten Medizin stehen Ärzte und Patienten dem Krebs nicht mehr machtlos gegenüber, wie noch vor wenigen Jahren.
©iStock / Marcin Klapczynski
In allererster Linie konzentriert sich die Krebstherapie auf drei Hauptsäulen:
- Operation
- Chemotherapie
- Strahlentherapie
Sie richten sich direkt gegen die krankhaften Zellen. Aber auch moderne Methoden wie Immuntherapien (z. B. CAR-T-Zellen) kommen zum Zuge bei der Behandlung von Tumoren und ihren Metastasen.
Strahlentherapie: Krebs-Klassiker mit moderner Präzision
Die Behandlung von Krebs mittels Strahlentherapie, bei der ionisierende Strahlen oder Teilchenstrahlung das Erbgut von Zellen schädigt, um sie an weiterer Zellteilung zu hindern, gilt seit Beginn des 20. Jahrhunderts als eine der effektivsten Methoden, um Tumore zu schrumpfen oder verschwinden zu lassen. Die Strahlung schädigt allerdings auch gesunde Zellen. Anders als ihre kranken Pendants haben sie jedoch – je nach Schweregrad der Schädigung – eher die Möglichkeit zur Reparatur. Während die Krebszellen absterben, soll sich das gesunde Gewebe von selbst regenerieren.
Aus diesem Grund wird die Strahlendosis traditionell über mehrere Sitzungen, sogenannte Fraktionen, verabreicht: Um dem gesunden Gewebe Zeit zu geben, sich zwischen den Behandlungssitzungen zu erholen. Weil der Kollateralschaden trotzdem groß war, geriet die Strahlentherapie um die Jahrtausendwende etwas außer Mode.
Moderne Systeme wie das CyberKnife sind in der Lage, millimetergenau einen Punkt im Körper aus verschiedenen Richtungen gleichzeitig zu treffen. Jeder einzelne Strahl ist zu schwach, um Gewebe ernsthaft zu schädigen. Nur der durch präzise Bildgebung bestimmte Punkt, an dem die Strahlen aufeinandertreffen, bekommt „die volle Ladung“ – und wird abladiert, medizinisch für eliminiert. Inzwischen wird der Strahlentherapie in der Krebsforschung wieder eine große Zukunft attestiert. Weitere Stichworte sind intensitätsmodulierte Strahlentherapie und die bildgesteuerte Strahlentherapie.

©iStock / Amornrat Phuchom
Chemotherapie: Gift für die schnellen Krebs-Zellen
Die Chemotherapie nutzt chemische Substanzen zur Behandlung bösartiger Tumoren. Dabei handelt es sich um Chemotherapeutika und Zytostatika (griech. kytos = Zelle; statikos = zum Stehen bringend). Diese Substanzen greifen in den Vermehrungszyklus der Krebszellen ein.
Der deutsche Mediziner und Forscher Paul Ehrlich (1854–1915), Medizin-Nobelpreisträger des Jahres 1908 und Namensgeber des Paul-Ehrlich-Instituts, gilt als Mitbegründer der Chemotherapie. Ehrlich ging es zum damalign Zeitpunkt allerdings nicht konkret um die Behandlung von Krebserkrankungen, sondern generell die Bekämpfung von Infektionskrankheiten mit wirksamen chemischen Substanzen. Er entwickelte ein Verfahren, um die Wirkung natürlicher Stoffe zu analysieren und dann gezielt synthetisch weiterzuentwickeln. Für die Entwicklung von Krebs-Medikamenten wurde diese Methode schließlich Anfang des 20. Jahrhunderts übernommen.
Bei allen Chemotherapie-Arten werden dem Körper – meistens über eine venöse Infusion – Zellengifte zugeführt. Seltener ist die Verabreichung in Tablettenform. Es gibt viele verschiedene Zytostatika, die oft miteinander kombiniert werden.
Da die Medikamente über den Blutkreislauf transportiert werden, wirken sie in der Regel im gesamten Körper. Spezielle Chemotherapeutika können selbst das Gehirn, das normalerweise durch die Blut-Hirn-Schranke geschützt ist, erreichen. Grund: Bei bösartigen Gehirntumoren ist die Schutzschranke sehr häufig gestört. Dadurch können auch Krebszellen erreicht werden, die bei Untersuchungen unentdeckt blieben und mit Operation oder Bestrahlung nicht gezielt behandelt wurden. Fachleute sprechen bei dieser Art der Therapie auch von einer systemischen Behandlung.
Die Toxine, also Zellengifte, sind so konzipiert, dass sie hauptsächlich schnell nachwachsende Zellen abtöten. Haare fallen deswegen fast immer aus. Aber auch Mund- und Darmschleimhäute sowie die Haut sind häufig betroffen. Durchfall, Rötungen, Juckreiz und Entzündungen sind typische Nebenwirkungen. Besonders schwerwiegend ist die Schädigung des Knochenmarks. Es produziert weniger weiße und rote Blutkörperchen, was zu Infektanfälligkeit und Blutarmut führen kann.

©iStock / ArtemisDiana
mRNA-Krebstherapie: Immuntherapie gegen Krebs
mRNA und die damit entwickelten Impfstoffe nahmen der Corona-Pandemie ein wenig von ihrem Schrecken. In einer von Biontech initiierten Studie werden mRNA-Impfstoffe aktuell unter anderem auch bei Darmkrebs getestet. Das Prinzip ist das gleiche wie bei der Corona-Impfung. „Der COVID-Impfstoff war für Biontech ein Easy Game, ein leichtes Spiel“, sagt Prof. Dr. Dirk Arnold, Ärztlicher Direktor des Asklepios Tumorzentrums Hamburg (ATZHH), der mit seinem Team ebenfalls mit dem mRNA-Impfstoff forscht. „Es gab nur einen Gegenspieler, das – abgesehen von Mutanten – immer gleiche Coronavirus. In der Onkologie ist das sehr viel komplizierter, denn jede Krebsart hat ihre eigene Genetik – die dann auch von Patienten zu Patienten sehr unterschiedlich ist.“
Im Prinzip funktioniert die mRNA-Impfung so, dass in der Teeküche des Immunsystems (medikamentös) ein Fahndungsplakat mit der Genetik des Tumors aufgehängt wird. Die Idee: Wenn die körpereigene Abwehr weiß, wie die getarnten Tumorzellen aussehen, kann es auch aktiv werden und diese aus dem Verkehr ziehen.
„Die mRNA-Vakzinierung ist nur eine von verschiedenen Immuntherapien, die in der modernen Onkologie erfolgreich zum Einsatz kommen“, sagt Onkologe Prof. Arnold. „Sie könnte ein weiterer Baustein in unserem Therapeutika-Instrumentarium werden.“
Noch ist die Forschung weit davon entfernt, eine Krebserkrankung mit einer mRNA-Impfung in den Griff zu bekommen. „Man wird damit noch keinen großen Primärtumor therapieren oder eine ausgedehnte Metastasierung heilen können“, so Prof. Dirk Arnold. „Wir konzentrieren uns im ersten Schritt auf Patienten, die nach OP und Chemo noch Restmengen von Tumor-DNA im Blut haben.“

©iStock / Meletios Verras
CAR-T-Zell-Therapie: programmierte T-Zellen im Einsatz gegen Krebs
Bei der CAR-T-Zell-Therapie (Chimeric-Antigen-Receptor-T-Zell-Therapie) entnehmen Mediziner dem Patienten Blut und isolieren daraus weiße Blutkörperchen, sogenannte T-Zellen. Diese werden außerhalb des Körpers so programmiert, dass sie bisher unsichtbare Tumorzellen erkennen und unschädlich machen können, sobald sie wieder injiziert worden sind. Dabei gelingt es den modifizierten T-Zellen, gesunde von kranken Zellen zu unterscheiden.
CAR-T-Zell-Therapie ist eine erst 2018 zugelassene Behandlungsform. Wie bei der mRNA-Vakzinierung muss die Therapie auf jeden Patienten individuell und aufwendig zugeschnitten werden. So individuell, dass nicht einmal Spenderblut oder das Blut eines anderen Krebserkrankten für die Gewinnung der noch nicht programmierten T-Zellen verwendet werden kann.
In Studien hat sich die CAR-T-Zell-Therapie für wenige und ausgewählte Patienten mit bestimmten Blut- oder Lymphdrüsentumoren bewährt. Sie wird nur in hochqualifizierten onkologischen Schwerpunktzentren angeboten.
Irreversible Elektroporation (IRE) bei Prostatakrebs: NanoKnife für die Potenz
Das NanoKnife kann Männer vor Impotenz und Inkontinenz retten. „Während bei den herkömmlichen Methoden bis zu 80 Prozent der Männer impotent und bis zu 50 Prozent inkontinent werden, lassen sich solch gravierende Nebenwirkungen mit dem NanoKnife grundsätzlich vermeiden“, sagt Prof. Dr. med. Dr. phil. Dr. med. habil. Michael K. Stehling. Der Urologe, Radiologe und Physiker hat seit 2011 in dem von ihm gegründeten Vitus Prostata Center in Offenburg mehr als 1.400 Männer erfolgreich behandelt und gilt als weltweit führender Experte für die NanoKnife-Therapie bei Prostatakrebs.
Herkömmliche Methoden sind die operative Entfernung der Prostata (radikale Prostatektomie) oder die lokal-ablativen Zerstörung der Vorsteherdrüse – wahlweise durch Hitze (hochintensiver fokussierter Ultraschall, kurz HIFU), Kälte (Kryotherapie) oder Bestrahlung (u. a. Protonentherapie, Brachytherapie).
„Die Region um die Prostata ist äußerst sensibel mit Organen und Nerven auf engstem Raum“, erklärt Prof. Stehling. Dazu gehören Harnröhre, Schließmuskel sowie Nerven für Erektion und Kontinenz. „Ein falscher Schnitt und diese Strukturen sind unwiderruflich zerstört.“ Mit der Irreversiblen Elektroporation kann so etwas nicht passieren. Das Geheimnis dieser Methode: ultrakurze Stromstöße, die lediglich Krebszellen zerstören. Gefäße, Bindegewebe und vor allem Nerven überstehen den Eingriff unbeschadet.“
Der IRE-Eingriff ist auch deutlich weniger belastend für den Körper als zum Beispiel die radikale Prostatektomie. Die Patienten können die Klinik schon am Folgetag verlassen und nach zwei Wochen wieder Sport machen.
Die Zahlen des Vitus Prostata Center belegen das eindrucksvoll: kein Patient inkontinent, weniger als 10 Prozent impotent. Das Bundesministerium für Gesundheit hat das NanoKnife vor wenigen Jahren offiziell als Therapie bei Prostatakrebs anerkannt. Inzwischen wird das NanoKnife auch bei anderen Krebsarten eingesetzt. Erste Erfolge hat zum Beispiel Prof. Dr. med. Dr. h.c. Tobias Keck, Direktor der Klinik für Chirurgie am Universitätsklinikum Schleswig-Holstein (UKSH) in Lübeck, bei Bauchspeicheldrüsenkrebs mit dem NanoKnife gemacht.
Krebs-Forschung: Neue Studienergebnisse zu Prostatakrebs
Wissenschafts- / Medizinjournalistin

Dr. rer. nat. Miriam Sonnet
Lutetium-177–PSMA-617
Männern mit metastasierten Prostatatumoren steht möglicherweise bald eine neue Therapieoption zur Verfügung. Die Behandlung mit 177Lu–PSMA-617 verlängerte die Zeit, in der die Erkrankung nicht voranschritt, deutlich im Vergleich zu einer Standardtherapie. Auch lebten die Betroffenen mit der neuen Methode länger. In den USA wurde sie von der FDA bereits zugelassen.
Ein Prostatatumor ist die häufigste Krebserkrankung bei Männern: Jährlich erkranken rund 65.000 Männer daran.[1] Die Therapie hängt maßgeblich davon ab, in welchem Stadium die Betroffenen ihre Diagnose erhalten. Häufig werden die Patienten operiert oder bestrahlt. Ist der Krebs bereits fortgeschritten, das heißt sind Lymphknoten befallen oder hat der Tumor in andere Organe gestreut, reicht meist eine Operation oder Bestrahlung nicht mehr aus. Die Betroffenen erhalten dann eine Therapie, die sich gegen alle im Körper vorliegenden Tumorzellen richtet – eine sogenannte systemische Behandlung. Hier kommen zum Beispiel Medikamente infrage, die den Hormonspiegel beeinflussen. Alternativ kann eine Chemotherapie zum Einsatz kommen.[2]
Eine neue Methode, um Erkrankte zu behandeln, ist die Anwendung von Lutetium-177 (177Lu)–PSMA-617. Dabei werden radioaktive Beta-Partikel in Prostatakrebszellen (und ihre Umgebung) eingeschleust, woraufhin diese absterben.[3]
Die amerikanische Zulassungsbehörde FDA (Food and Drug Administration) hat die Therapie bereits im März 2022 zugelassen. Die Zulassung basiert auf den Ergebnissen der Studie VISION III, in der 177Lu–PSMA-617 bei Männern mit einer bestimmten Form von metastasiertem Prostatakrebs geprüft wurde.[4]
Info: 177Lu–PSMA-617
Bei 177Lu–PSMA-617 ist radioaktives Lutetium-177 an einen Liganden gekoppelt. Letzterer kann an eine Struktur andocken, die häufig auf Prostatakrebszellen zu finden ist: das Prostata-spezifische Membranantigen, kurz PSMA. Die Tumorzellen nehmen 177Lu–PSMA-617 auf, dieses gibt folglich von innen heraus seine Strahlendosis ab, was Krebszellen eliminiert. Die Behandlung ist damit sehr zielgenau auf Prostatakrebszellen zugeschnitten.[4]
Studiendesign: 831 Patienten erhielten entweder 177Lu–PSMA-617 plus eine Standardtherapie oder eine alleinige Standardtherapie.
Teilnehmer der Studie: Die Teilnehmer waren an einer bestimmten Form des metastasierten Prostatakarzinoms erkrankt und vor der Studie bereits mit verschiedenen Medikamenten behandelt worden.
Die Therapie verlängerte die Zeit, in der die Erkrankung nicht voranschritt (= progressionsfreies Überleben). Median lebten die Patienten unter der 177Lu–PSMA-617 8,7 Monate und in der Kontrollgruppe 3,4 Monate ohne Progress. Auch lebten die Teilnehmer des 177Lu–PSMA-617-Studienarms median länger als die Betroffenen, die eine Standardtherapie erhalten hatten (Gesamtüberleben 15,3 Monate vs. 11,3 Monate).
Häufige Nebenwirkungen unter 177Lu–PSMA-617 umfassten Fatigue (extreme Müdigkeit, eine häufige bei Krebstherapien auftretende Nebenwirkung), Mundtrockenheit und Übelkeit. Nebenwirkungen vom Schweregrad 3 oder höher traten unter 177Lu–PSMA-617 öfter auf als unter der Standardtherapie. Die Lebensqualität der Teilnehmer verschlechterte sich dadurch aber nicht.
Fazit: Die Behandlung mit 177Lu–PSMA-617 verlängerte die Zeit, in der ein metastasiertes Prostatakarzinom nicht voranschritt, schreiben die Autoren in ihrem Fazit. Auch das Gesamtüberleben der betroffenen Männer wurde verlängert.
[1] https://www.krebsinformationsdienst.de/tumorarten/prostatakrebs/anatomie-krebsentstehung-haeufigkeit.php (letzter Aufruf am 20.4.2022)
[2] https://www.krebsinformationsdienst.de/tumorarten/prostatakrebs/behandlung.php (letzter Aufruf am 20.4.2022)
[3] Sartor O et al. N Engl J Med 2021; 385:1091-1103
[4] https://www.gesundheitsindustrie-bw.de/fachbeitrag/pm/fda-zulassung-fuer-therapeutikum-gegen-metastasierten-prostatakrebs (letzter Aufruf am 20.4.2022)

©iStock / CIPhotos
Analyse der Tumor-DNA: präzise Ergebnisse aus dem Labor
Nicht nur neue Medikamente und technische Innovationen geben Hoffnung. Die Behandlung von Krebs wird immer zielgenauer auf die Patienten zugeschnitten. Das bezeichnen Ärzte auch mit dem Begriff „personalisierte Medizin“. Der Hintergrund ist, dass jeder Tumor ganz individuelle Eigenschaften besitzt. Verschiedene Patienten sprechen daher auch unterschiedlich gut auf einzelne Wirkstoffe an.
Mithilfe der Sequenzierung ist es heute möglich, bösartige Geschwulste genauestens im Labor zu charakterisieren und Veränderungen im Erbgut aufzuspüren. Das wiederum hilft dabei, die Behandlung individuell auf den jeweiligen Tumor und Patienten auszurichten. Mittlerweile gibt es für einige Krebsarten zielgerichtete Medikamente, die genau auf diese Veränderungen reagieren.
Beispiel ist der Wirkstoff Trastuzumab, ein Eiweißstoff, der einen bestimmten Tumorfaktor ausschaltet und somit das Wachstum bremst. Das Präparat kommt bei Brustkrebs zum Einsatz, aber nur dann, wenn der Faktor, auf den es abzielt, auch tatsächlich vorhanden ist.
Karzinomgenetik: natürlicher Zelltod
Tochtergeschwulste, medizinisch Metastasen, machen den Krebs so gefährlich. Ableger, die sich ausbreiten, sind die häufigste Todesursache bei Krebserkrankungen. Forscher aus der Schweiz haben eine Art Barriere identifiziert, die den Krebs von der Metastasierung abhält. Diese besteht aus einem Protein mit der Bezeichnung Activin B und dem Rezeptor ALK7. Die Kombination Activin B und ALK7 bildet einen Signalweg, durch den Krebszellen auf natürliche Weise absterben (Apoptose). So könnte nicht nur die Entstehung des Tumors selbst, sondern die seiner Tochterzellen bekämpft werden. Die Entdeckung dieser Barriere könnte ein vielversprechendes Ziel für Arzneimittel gegen Krebs sein.
Einen anderen Ansatz verfolgen Wissenschaftler am Deutschen Krebsforschungszentrum in Heidelberg. In Laborversuchen fanden sie heraus, dass Metastasen ausgehungert werden können. Um sich in einem fremden Organ anzusiedeln, müssen sich die Geschwulste an dessen Stoffwechsel anpassen. Wird dieser aber gestört – zum Beispiel indem Fettsäuren nicht mehr aufgenommen werden können – sterben die Metastasen ab. Ob diese Anwendung auch beim Menschen möglich ist, müssen weitere Studien zeigen.

Hautkrebs: Es war ein Mal
Muss jede Veränderung auf der Haut sofort operativ entfernt werden? Nicht jede – aber wo interveniert werden muss, sollte unbedingt ein Dermatologe entscheiden.
Sonne pur und unter Palmen die Seele baumeln lassen – viele Deutsche erholen sich in den Ferien am liebsten am Strand. Gut eingecremt, wähnt sich der Urlauber auf der sicheren Seite und genießt die wärmenden Strahlen. Schöner Nebeneffekt, der anschließend mit nach Hause gebracht wird, ist die Sonnenbräune. Doch jede Minute, in der die Haut die pralle UV-Dosis bekommt, erhöht das Risiko, an Hautkrebs zu erkranken. Darum ist es gerade in den Wochen oder Monaten nach dem Urlaub wichtig, zur Vorsorge zu gehen. Denn die meisten Hautkrebsarten sind in ihren Anfangsstadien noch gut heilbar.
©iStock / koto_feja
Weißer Hautkrebs ist schwer zu erkennen
Laut eines Berichts der Techniker Krankenkasse erkranken im Jahr etwa 270.000 Menschen in Deutschland an Hautkrebs, der Großteil davon, circa 230.000 Patienten, allerdings nicht am gefährlichen schwarzen Hautkrebs (malignes Melanom), der sich durch dunkle Verfärbungen äußert, sondern an den weißen Formen der Krankheit. 80 Prozent davon am Basalzellkarzinom, auch Basaliom genannt, der Rest am Plattenepithelkarzinom (Stachelzellkarzinom).
Besonders anfällig für weißen Hautkrebs sind Hautstellen wie die sogenannten „Sonnenterrassen“ des Körpers, also Gesicht, Hände oder bei Frauen das Dekolleté, die über viele Jahre der UV-Strahlung besonders ausgesetzt waren. Da diese Tumoren selten metastasieren, sind sie in der Regel weniger lebensgefährlich als das schwarze Melanom. Metastasen entstehen hier nur dann, wenn das Immunsystem des Betroffenen aufgrund von Vorerkrankungen medikamentös unterdrückt wird oder das Karzinom lange unentdeckt bleibt. Je früher also erkannt, desto besser stehen die Heilungschancen bei beiden Formen des hellen Hautkrebses: Er lässt sich einfach herausschneiden, bestrahlen, vereisen, weglasern oder durch spezielle Cremes entfernen.
Doch das Problem ist die prophylaktische Diagnose, den Krebs erkennen. Denn anders als das maligne Melanom, der schwarze Hautkrebs, sind die weißen Varianten schwerer auszumachen. Beim Plattenepithelkarzinom entstehen unscheinbare hautfarbene Flecken, die zum Beispiel einem schlecht verheilten Insektenstich oder einer kleinen Narbe ähneln. Nur selten vermutet der Betroffene dahinter schon eine Vorstufe von Krebs. Auch schuppige Stellen oder Wunden, die immer wieder aufbrechen, sollte ein Hautarzt genauer begutachten.

©iStock / Md Saiful Islam Khan
Gute Prognosen trotz bösem Krebs-Befund
Das Basaliom dagegen hat keine Vorstufe. Es ist oft hell, manchmal auch dunkel pigmentiert. Außerdem ist es nicht selten von einem perlschnurartigem Randsaum umgeben und bildet einen Knoten, der bluten kann. Hier sollte das Geschwür durch einen operativen Eingriff entfernt werden, bevor es sich vergrößern und tiefere Hautschichten befallen kann.
Ein malignes Melanom kann überall am Körper auftreten – auch an Stellen, die kaum oder gar nicht der Sonne ausgesetzt sind. Diese Geschwüre können meistens im frühen Stadium unkompliziert aus der Haut geschnitten werden. Schwieriger wird es, sobald der Tumor in tiefere Schichten eindringt und in Lymphknoten, Leber, Lunge oder Gehirn streut.
Bei einem solchen Befund ist die Immuntherapie im Anschluss an die OP inzwischen die Behandlung der Wahl. Hierbei erhält der Patient über die Armvene spezielle Antikörper. Die sogenannten Checkpoint-Inhibitoren wie Nivolumab und Ipilimumab helfen der körpereigenen Abwehr, entartete Zellen zu identifizieren und zu bekämpfen. Auch der metastasierte weiße Hautkrebs hat gegen die Immuntherapie oft keine Chance.
Ganzkörper-Check alle zwei Jahre
Doch damit es erst gar nicht so weit kommt, raten Experten zum Früherkennungs-Check. Dabei sucht der Arzt den kompletten Körper inklusive Kopf nach verdächtigen Stellen ab. Alle zwei Jahre bezahlen die gesetzlichen Krankenkassen Versicherten ab 35 Jahren dieses Hautkrebsscreening. Manche Kassen bieten sie auch Jüngeren an.
Geübte Dermatologen inspizieren die Haut nach Auffälligkeiten und schauen im Zweifel genauer hin. Letzte Sicherheit bietet in modernen dermatologischen Praxen ein Abgleich mit dem Rechner, der im Zweifel auch Auffälligkeiten entdeckt, wo der Arzt sie nicht sieht.
Jeder Einzelne sollte aber selbst persönliche Vorsorge treffen. Das bedeutet: Die pralle Mittagssonne meiden, und zwar nicht nur im Sommer. Aus dem Sortiment an Sonnen-Cremes die mit einem hohen Lichtschutzfaktor wählen. Noch besser schirmt Kleidung die Strahlung ab – besonders dunkle und dichtfaserige. Außerdem kennen viele Menschen ihre Muttermale. Daher ist es ratsam, ein Mal im Monat bei Tageslicht nach ungewöhnlichen Veränderungen an seinem Körper Ausschau zu halten.
Neue Studien zufolge können auch Lebensmittel, die viel Vitamin A enthalten wie Eier oder Leber sowie karotinhaltige Produkte wie Karotten, Kürbis oder Kohl helfen, vor Hautkrebs zu schützen.
Krebs-Forschung: Neue Studienergebnisse zu Hautkrebs
Wissenschafts- / Medizinjournalistin

Dr. rer. nat. Miriam Sonnet
Zweifach-Therapie mit Immutherapeutika
Immuntherapeutika kommen bereits seit längerer Zeit zur Therapie des schwarzen Hautkrebses zum Einsatz. In einer kürzlich veröffentlichten Studie wurde ein neuer Wirkstoff (Relatlimab) in Kombination mit einem weiteren Immuntherapeutikum bei zuvor unbehandelten Patienten untersucht. Die Zweifach-Therapie verlängerte das progressionsfreie Überleben der Teilnehmer, also die Zeit, in der die Erkrankung nicht voranschritt.
Im Jahr 2018 erkrankten rund 23.000 Menschen an einem Melanom – dem schwarzen Hautkrebs. Nach wie vor stellt die Operation die wichtigste Therapieform dar. Teilweise kommt aber auch eine Bestrahlung zum Einsatz. Neuere Methoden umfassen die Immuntherapie und zielgerichtete Substanzen.[1]
Unter dem Begriff „Immuntherapie“ versteht man alle Strategien, die die körpereigenen Abwehrkräfte nutzen, um Krebs zu bekämpfen. Eine Möglichkeit besteht darin, Medikamente einzusetzen, die sich gegen „Bremsen“ (engl. Checkpoints) des Immunsystems richten. Diese haben normalerweise die Aufgabe, überschießende Reaktionen des Immunsystems zu verhindern. Einige Tumoren aktivieren diese Checkpoints – das Immunsystem wird dadurch geschwächt und es kann die Krebszellen nicht mehr erkennen. Hier kommen Substanzen wie Checkpoint-Inhibitoren ins Spiel: Sie blockieren die Checkpoints, woraufhin die Immunantwort nicht mehr unterdrückt wird. Die körpereigene Abwehr kann somit den Tumor angreifen.[2]
Inzwischen gibt es mehrere Checkpoint-Inhibitoren, die beim Melanom und anderen Krebsarten eingesetzt werden können. Die Wirksamkeit einer neuen Substanz dieser Art (Relatlimab) wurde kürzlich in einer Studie (RELATIVITY-047) bei Patienten geprüft, die zuvor noch keine Therapie für ihren Hautkrebs erhalten hatten. Das Medikament kam darin in Kombination mit einem anderen immuntherapeutischen Wirkstoff (Nivolumab) zum Einsatz. Nivolumab ist bereits zur Behandlung von schwarzem Hautkrebs zugelassen.
Info: Angriffspunkte von Relatlimab und Nivolumab
Relatlimab bindet an ein spezifisches Oberflächenmolekül auf bestimmten Immunzellen: LAG-3. Dieses kontrolliert unter anderem das Wachstum und die Aktivierung der Zellen. Werden LAG und der dahinterstehende Signalweg gehemmt, so kann das erschöpfte Immunzellen wieder aktivieren und Reaktionen gegen Tumoren fördern.[3]
Nivolumab bindet an den Checkpoint PD-1. Auch PD-1 hemmt die Funktion bestimmter Immunzellen, was überschießende Reaktionen der körpereigenen Abwehr verhindern soll. Wird der PD-1 Checkpoint durch Nivolumab blockiert, aktiviert das Immunzellen und erhöht deren Fähigkeit, Tumoren zu eliminieren.[4, 5]
Studiendesign: Bereits zuvor wurde die Wirksamkeit von Relatlimab in Kombination mit Nivolumab bei Patienten mit Melanomen, die bereits mit anderen Medikamenten / Therapien vorbehandelt waren, geprüft und bestätigt. Unklar war bisher, ob auch Personen, die noch nicht aufgrund ihres Melanoms behandelt worden waren, von der Zweifach-Kombination profitieren.
Die Teilnehmer wurden alle vier Wochen mit einer Kombination aus Relatlimab und Nivolumab mit fester Dosis behandelt. Die Therapie wurde intravenös verabreicht. Als Vergleichsgruppe dienten Erkrankte, die nur Nivolumab bekamen.
Geprüft werden sollte, ob die Kombination das progressionsfreie Überleben der Betroffenen verlängern kann. Als progressionsfreies Überleben wird die Zeit bezeichnet, in der die Erkrankung nicht voranschreitet oder sich verschlimmert.
Teilnehmer: Alle Patienten, die an der Studie teilnahmen, litten unter schwarzem Hautkrebs, der entweder nicht operiert werden konnte oder bereits Metastasen gebildet hatte.
Das mediane progressionsfreie Überleben betrug 10,1 Monate unter der Zweifach-Behandlung und 4,6 Monate unter alleiniger Nivolumab-Medikamentation. Statistisch gesehen hatten damit Patienten, die mit Relatlimab plus Nivolumab behandelt worden waren, ein um 25 % verringertes Risiko, dass die Erkrankung voranschritt. Nach zwölf Monaten lebten noch 47,7 % vs. 36 % der Teilnehmer ohne einen Krankheitsprogress.
Nebenwirkungen vom Schweregrad 3 oder 4 erlitten 18,9 % der Probanden, die Relatlimab plus Nivolumab erhalten hatten. In der Kontrollgruppe war dies bei 9,7 % der Betroffenen der Fall.
Fazit: Werden zwei Checkpoints durch spezifische Medikamente gehemmt, so bietet das für Erkrankte mit schwarzem Hautkrebs einen zusätzlichen Vorteil. Gleichzeitig traten unter der Kombinationstherapie keine neuen Nebenwirkungen auf.
[1] https://www.krebsinformationsdienst.de/tumorarten/hautkrebs.php. (Letzter Aufruf am 20.4.2022)
[2] https://www.krebsinformationsdienst.de/behandlung/immuntherapie/impfen-gegen-krebs.php (Letzter Aufruf am 20.4.2022)
[3] https://www.gelbe-liste.de/dermatologie/anti-lag-3-antikoerper-relatlimab-melanom (Letzter Aufruf am 20.4.2022)
[4] https://flexikon.doccheck.com/de/PD-1-Rezeptor#:~:text=Der%20PD%2D1%2DRezeptor%2C,programmed%20cell%20death%20protein%201%22. (Letzter Aufruf am 20.4.2022)
[5] https://www.cancer.gov/publications/dictionaries/cancer-terms/def/pd-1 (Letzter Aufruf am 20.4.2022)
[6] Tawbi HA et al. N Engl J Med 2022; 386:24-34

Leukämie: Lichtblick im Kampf gegen den Blutkrebs
Vor einem halben Jahrhundert war die Leukämie-Diagnose gleichbedeutend mit einem Todesurteil. Doch dank moderner Forschung stehen Patienten heute gute Behandlungsmöglichkeiten zur Verfügung. Über die Ursachen, die Leukämien entstehen lassen, herrscht bisher immer noch ein großes Rätselraten. Lediglich die verschiedenen Faktoren, die das Erkrankungsrisiko erhöhen, sind bekannt. Dazu gehören eine gewisse erbliche Belastung, radioaktive Strahlen und Röntgenstrahlen sowie bestimmte chemische Substanzen. Doch der Wissenschaft ist es gelungen, erfolgreiche Therapien zu entwickeln, die eine Heilung in greifbare Nähe rücken lassen.
©iStock / wildpixel
Weiße Blutkörperchen geraten außer Kontrolle
Der herkömmliche Entwicklungspeifungsprozess weißer Blutkörperchen (Leukozyten) im Knochenmark kann durch eine Fehlschaltung spezifischer Kontrollgene unterbrochen werden. Dann entsteht Krebs: Anstelle von vollständig entwickelten und funktionstüchtigen Leukozyten bilden sich mehr oder weniger unausgereifte Blutkörperchen. Diese sind in der Regel nicht funktionsfähig, vermehren sich rasch und unkontrolliert, sodass sie zunehmend die gesunden roten und weißen Blutkörperchen verdrängen.

©iStock / stefanamer
Blässe und Abgeschlagenheit als mögliche Krebs-Symptome
Der Begriff Leukämie bedeutet „weißes Blut“ und entstand aus der Beobachtung einer Vermehrung von weißen Blutkörperchen im Blut. Dieser Begriff wurde erstmals 1845 von Rudolf Virchow verwendet und hat seitdem Eingang in die Medizin gefunden.
Das Tückische beim Blutkrebs: Die Symptome sind die gleichen, wie sie bei anderen, weitaus harmloseren Erkrankungen vorkommen können. Dazu zählen Blässe, häufige Infekte und spontanes Nasenbluten. Viele Leukämie-Patienten berichten aber auch von einer plötzlichen Abgeschlagenheit, die sie sich nicht erklären konnten. Wer also häufig müde ist und sich dies nicht erklären kann, sollte eine Blutuntersuchung beim Arzt in Erwägung ziehen.
Chemo und demethylierende Wirkstoffe
Ist die Diagnose eindeutig, wird mit einer Chemotherapie versucht, möglichst alle Krebszellen zu zerstören. Zusätzlich bekommen einige Patienten noch Antikörper. Jeder Mensch trägt Antikörper im Blut. Ihre Aufgabe ist es, Erreger wie Viren und Bakterien aufzuspüren. Sie lassen sich aber auch künstlich herstellen und so verändern, dass sie Krebszellen erkennen und attackieren können.
Während bei der Chemo Krebszellen gezielt zerstört werden, gehen demethylierende Substanzen wie Aacidtidin und Decitabin noch tiefer in die molekulare Struktur. Sie können die Chemie der Gene so beeinflussen, dass die Leukämiezellen manipuliert werden und danach absterben. Studien haben bereits positive Effekte gezeigt, und es kommt zu deutlich weniger Nebenwirkungen. Demethylierende Mittel werden vor allem bei Leukämie-Patienten im Alter von über 65 Jahren verwendet, die keine Stammzelltransplantation erhalten können.

©iStock / Manjurul
Suche nach dem „genetischen Zwilling“
Eine Stammzellentransplantation ist zwingend notwendig, wenn ein Patient ein Rezidiv erleidet, also erneut erkrankt. Es zeigt sich aber häufig schon bei der Erstdiagnose, dass eine Chemo- oder Antikörpertherapie nicht ausreicht und eine Stammzellenbehandlung meist die letzte Überlebenschance ist.
Ziel ist es, erkranktes Knochenmark durch gesundes zu ersetzen. Zunächst wird eine Gewebeanalyse gemacht. Dann geht es auf die Suche nach einem Spender mit passenden Gewebemerkmalen. Dabei überprüft man zuerst Familienmitglieder, etwa die leiblichen Geschwister. Stimmen die Werte nicht überein, wird mittels Datenbank ein Fremdspender gesucht.
28 Millionen spendenwillige Menschen
Aufgrund zahlreicher Aktionen etwa in den Medien ist die Bereitschaft in der Bevölkerung zur Knochenmarkspende enorm gestiegen. Die Hämatologen können weltweit auf alle Spenderportale zugreifen, insgesamt 28 Millionen Menschen sind in der Datenbank erfasst. In 70 Prozent der Fälle wird ein Spender gefunden.
Vor einer Transplantation wird der Spender noch einmal gründlich untersucht. Dann entnehmen die Ärzte Stammzellen aus seinem Knochenmark und schicken sie der jeweiligen Klinik, die den Krebspatienten behandelt. Normalerweise lernen sich die Spender und Empfänger nicht kennen. Aber nach zwei Jahren haben die Betroffenen die Möglichkeit, die Anonymität aufzuheben. Die Deutsche Knochenmarkspenderdatei (DKMS) informiert, wie man spenden und Leben retten kann.

©iStock / mediaphotos
CAR-T-Zell-Therapie – bislang nur für Kinder und Jugendliche
Wissenschaftler haben die sogenannten CAR-T-Zell-Therapie auch für den Einsatz bei Leukämie im Blick. Hier werden Immunzellen gentechnisch so verändert, dass sie, ähnlich wie Antikörper, bösartige Zellen zerstören können. Sie ist momentan für Patienten unter 25 Jahren und nur für eine bestimmte Form der Leukämie, die akute lymphatische Leukämie (ALL – die häufigste Krankheitsform bei Kindern) zugelassen. Zwei Therapiezyklen müssen bereits erfolglos gewesen sein.
Problem: Der Eingriff kostet rund 250.000 Euro, weil viel Infrastruktur nötig ist, die es nur in an großen Krebszentren gibt. Aber: Die Behandlung zeigt Erfolg. Wenn es gelingt, den Aufwand zu minimieren, könnte das künftig eine vielversprechende Therapieform sein, hoffen die Ärzte.
Lebensstil verantwortlich für Leukämieentstehung?
Die Frage, ob es einen Zusammenhang zwischen Lebensstil und Krebsentstehung bei der Leukämie gibt, wird schon lange diskutiert, ist aber noch unklar. Denn es erkranken auch Kinder und Jugendliche, die in der Regel über ein sehr vitales Immunsystem verfügen. Eine ausgewogene Ernährung und regelmäßige Bewegung sind aber immer empfehlenswert.
Leukämie ist im eigentlichen Sinne nicht vererbbar. Allerdings haben Untersuchungen gezeigt, dass Menschen ein höheres Erkrankungsrisiko haben, wenn es innerhalb der Familie bereits bösartige Tumorfälle gab.
Krebs-Forschung: Neue Studienergebnisse zu Hodgkin-Lymphomen
Wissenschafts- / Medizinjournalistin

Dr. rer. nat. Miriam Sonnet
CAR-T-Zell-Therapie
Die CAR-T-Zell-Therapie hat kürzlich das Behandlungsspektrum mancher Krebsarten erweitert und Ärzte erzielen damit bei ihren Patienten beachtliche Erfolge. Die Herstellung der CAR-T-Zellen ist allerdings sehr aufwendig und erfolgt individuell für jeden Betroffenen. In Europa gibt es bislang zwei zugelassene Produkte für bestimmte Tumorarten. Auch für Erkrankte mit Hodgkin-Lymphom scheint die Therapie wirksam zu sein und Forscher versuchen, die Effektivität durch verschiedene Tricks weiter zu steigern.
Das Hodgkin-Lymphom ist eine seltene Krebserkrankung. Aktuellen Daten zufolge erkrankten 1.100 Frauen und 1.440 Männer in Deutschland im Jahr 2018 neu daran.[1] Ursache des Hodgkin-Lymphoms sind Veränderungen in bestimmten weißen Blutzellen, den B-Zellen. Diese teilen sich ungebremst und vermehren sich schneller als normale Körperzellen, wodurch gesundes Gewebe verdrängt wird. Zunächst vermehren sich die veränderten Zellen in den Lymphknoten. Die Erkrankung kann sich aber auch im gesamten Körper ausbreiten und andere Organe außerhalb des lymphatischen Systems befallen.[2]
Info: Lymphatisches System und Lymphome
Als Lymphome werden in der Regel bösartige Tumoren des lymphatischen Systems bezeichnet. Das lymphatische System ist über den gesamten Körper verteilt und besteht aus Lymphbahnen, die Lymphe (Gewebswasser) transportieren, und aus den lymphatischen Organen, unter anderem Thymus und Knochenmark.[2] Das lymphatische System steht in engem Zusammenhang mit dem Immunsystem und dem blutbildenden System.[3]
Die „Lymphozyten“ sind die Zellen des lymphatischen Systems. Es handelt sich dabei um eine Gruppe weißer Blutkörperchen. Sie spielen eine wichtige Rolle bei der Immunabwehr und können Krankheitserreger erkennen und eliminieren. Es gibt zwei große Gruppen von Lymphozyten: B- und T-Zellen.[3]
Bei einem Lymphom entarten die Lymphozyten, sie wachsen unkontrolliert und vermehrten sich. Typisches Warnzeichen der Erkrankung ist eine schmerzlose Lymphknotenschwellung. Weitere Beschwerden, die auftreten können, umfassen unter anderem Fieber, starken Nachtschweiß und ungewollten Gewichtsverlust.[4]
Bösartige Lymphome können grob in drei Untergruppen unterteilt werden[4]:
1. Hodgkin-Lymphome
2. Non-Hodgkin-Lymphome
3. Multiples Myelom
Obwohl Hodgkin-Lymphom-Patienten mit einer ersten Therapie eine gute Prognose haben, erleiden rund 20 % bis 30 % der Betroffenen einen Rückfall der Erkrankung. Für eine erneute Behandlung kommt dann meist eine hochdosierte Chemotherapie und eine anschließende Stammzelltransplantation zum Einsatz.[5]
Stammzelltransplantation
Erleidet ein Hodgkin-Patient einen Krankheits-Rückfall, erhält er oft eine hochdosierte Chemotherapie, welche die Krebszellen vernichten soll. Dabei werden allerdings auch die normalen blutbildenden Zellen, die sogenannten Blutstammzellen, angegriffen. Ärzte entnehmen diese dem Betroffenen daher vor der Chemotherapie und geben sie ihm nach der Chemo zurück. So kann der Körper aus den Blutstammzellen wieder Blutzellen bilden. Dieses Verfahren heißt „autologe Stammzelltransplantation“.[2]
In den vergangenen Jahren hat sich die moderne Krebstherapie gewandelt: Es werden vermehrt Ansätze erprobt, die Tumorzellen gezielt angreifen. Eine Revolution gelang unter anderem mit den CAR-T-Zellen. Die Herstellung dieses speziellen Produkts ist sehr aufwendig: Dem Patienten werden eigene T-Zellen entnommen und diese in einem Speziallabor genetisch so verändert, dass sie auf ihrer Oberfläche eine Struktur (Rezeptor) ausbilden, die bestimmte Eiweiße (Antigene) auf Tumorzellen erkennt. Der Patient erhält anschließend diese veränderten T-Zellen – die CAR-T-Zellen – wieder zurück, die dann den Krebs spezifisch erkennen und angreifen sollen. Die eingeführte Struktur auf den T-Zellen besteht aus mehreren Bausteinen, die normalerweise nicht zusammen auftreten, und wird daher als „chimär“ bezeichnet. Die Abkürzung „CAR“ steht für Chimärer Antigen Rezeptor.[6]
Zugelassen ist die CAR-T-Zell-Therapie bereits für bestimmte Situationen beim diffus großzellige B-Zell-Lymphom und akuten Leukämien. Auch für die Behandlung des Hodgkin-Lymphoms werden CAR-T-Zellen in verschiedenen Studien geprüft. Forscher versuchen in mehreren Ansätzen, die Wirksamkeit zu steigern. In einem neuen Review wurden die aktuellen Daten dazu zusammengefasst.[5]
Ein Fokus beim Hodgkin-Lymphom liegt zurzeit auf CAR-T-Zellen, die ein spezielles Eiweiß erkennen, das auf Hodgkin-Lymphomen vermehrt zu finden ist: Das sogenannte CD30-Antigen. Ein Vorteil: Dieses Eiweiß wird von normalen Zellen kaum ausgebildet und die entsprechend veränderten und auf CD30 „abgerichteten“ CAR-Ts wirken daher spezifisch auf die bösartigen Krebszellen. Das limitiert toxische Effekte auf gesundes Gewebe.[5]
CD30-CAR-T-Zellen: Forscher untersuchten in einer ersten Studie Wirksamkeit und Sicherheit der CD30-CAR-T-Zellen bei 18 Hodgkin-Lymphom-Patienten, die zuvor mit mehreren Therapien erfolglos behandelt worden waren. Die Teilnehmer vertrugen die Behandlung gut und bei sieben von ihnen bildete sich die Krankheit teilweise zurück (partielle Remission). Sechs Personen wiesen eine stabile Erkrankung auf, das heißt dass es keine Anzeichen für ein fortschreitendes Krebswachstum oder einen neuen Tumor gab.[7]
In einer weiteren Studie wurden die CD30-CAR-T-Zellen bei 41 Patienten geprüft. Auch hier hatten die Teilnehmer bereits mehrere vorangegangene Therapien hinter sich. Die Behandlung wurde erneut gut vertragen: Ein Zytokinfreisetzungssyndrom – eine gefürchtete Nebenwirkung der CAR-T-Zellen – war meist nur leicht ausgeprägt (Schweregrad 1). Neurologische Nebenwirkungen, die ebenfalls häufig im Zuge einer CAR-T-Zell-Therapie beobachtet werden, gab es nicht. Bei 72 % der Studienteilnehmer war die Behandlung mit den CAR-T-Zellen wirksam. 94 % überleben das erste Jahr nach der Therapie und in 36 % der Fälle schritt die Erkrankung innerhalb eines Jahres nicht weiter voran.[8]
Zytokinfreisetzungssyndrom: Systemische Entzündungsreaktion, bei der es zu einer massiven Freisetzung von Zytokinen kommt. Zytokine sind Moleküle, die im Körper verschiedene Prozesse regeln, unter anderem die Signalübertragung zwischen Zellen. Symptome des Zytokinfreisetzungssyndroms sind unter anderem Fieber, Übelkeit, Erbrechen, Durchfall, Blutdruckabfall, Krämpfe, Verwirrtheit und Herzrasen. In schweren Fällen kann es tödlich enden. (Quelle: https://flexikon.doccheck.com/)
Die Ergebnisse verdeutlichen, dass CAR-T-Zellen selbst für stark vorbehandelte Hodgkin-Lymphom-Patienten geeignet zu sein scheinen. Obwohl es mittlerweile mehr als 20 klinische Studien gibt, steckt die CAR-T-Zell-Therapie beim Hodgkin-Lymphom aber noch immer in den Kinderschuhen. Eine Frage, die Forscher beantworten müssen, ist unter anderem: Wie lässt sich die Effektivität der Behandlung erhöhen? Wissenschaftler prüfen dazu mehrere Strategien.[5]
1. Die Nutzung von T-Gedächtniszellen
Ein Problem der CAR-T-Zell-Behandlung: Ihre Beständigkeit reicht möglicherweise häufig nicht aus, um die Krebszellen vollständig zu eliminieren. Ein aktueller Ansatz besteht darin, ein CAR-T-Zell-Produkt zu verwenden, das mit „stammzellartigen Gedächtnis-T-Zellen“ angereichert ist. Das kann die Wirksamkeit der CART-Zellen erhöhen.[5]
2. Die Einwanderung in die Tumor-Mikroumgebung erhöhen
CAR-T-Zellen werden oftmals durch das die Tumoren umgebende Milieu daran gehindert, ihre volle Effektivität zu entfalten oder zu ihren Zielzellen zu gelangen. Schuld sind unter anderem bestimmte Moleküle, welche die normale Funktion des Immunsystems unterdrücken. Es gibt Hinweise darauf, dass man die genetisch veränderten T-Zellen weiter so modifizieren kann, dass sie leichter in die Tumor-Mikroumgebung gelangen können. Mit dieser Methode wurden in einer ersten Studie bereits acht Hodgkin-Lymphom-Patienten behandelt. Die speziellen CAR-T-Zellen zeigten bei allen Teilnehmern eine gewisse Wirksamkeit.[9]
3. Kombination mit anderen Therapien
Patienten, die CAR-T-Zellen erhalten haben, profitieren möglicherweise von einer weiteren, relativ neuen Behandlungsart: Den Checkpoint-Inhibitoren. Dabei handelt es sich um Medikamente, die das Immunsystem scharf gegen den Krebs stellen, sodass es den Tumor angreift und zerstört. In einer aktuellen Studie erhielten fünf Erkrankte, bei denen das Hodgkin-Lymphom nach einer CAR-T-Zell-Therapie vorangeschritten war, einen Checkpoint-Inhibitor. Die Studienautoren konnten bei allen Teilnehmern eine gewisse Wirksamkeit nachweisen. Die Strategie sollte in weiteren Studien geprüft werden, schlussfolgern die Forscher.[10] Denkbar ist auch die direkte Kombination aus Checkpoint-Inhibitoren und CAR-T-Zellen.[5]
Die Behandlungsmöglichkeiten für Hodgkin-Lymphom-Patienten haben sich dank einer Reihe von neuen Strategien maßgeblich geändert. CAR-T-Zellen sind eine vielversprechende Strategie, die selbst bei sehr stark vorbehandelten Erkrankten effektiv zu sein scheint. Wie die CAR-T-Zellen allerdings in die derzeitigen Therapiekonzepte integriert werden sollen, müssen Mediziner noch prüfen. Ermutigend ist nicht nur die Wirksamkeit von CD30-CAR-T-Zellen, sondern auch ihre begrenzte Toxizität.[5]
Bisher zugelassene CAR-T-Zell-Therapien bei anderen Krebsarten
Bisher gibt es in Europa zwei zugelassene CAR-T-Zell-Produkte (Stand April 2022):
Tisagenlecleucel ist zugelassen für die Therapie von
– Kindern, Jugendlichen und jungen erwachsenen Patienten im Alter bis einschließlich 25 Jahre mit refraktärer* oder rezidivierter** (Rezidiv nach Transplantation oder zweites oder späteres Rezidiv) akuter lymphatischer B-Zell-Leukämie (ALL)
– erwachsenen Patienten mit rezidiviertem oder refraktärem diffus großzelligen B-Zell-Lymphom (DLBCL) nach zwei oder mehr Linien einer systemischen Therapie***
Das DLBCL gehört zu den Non-Hodgkin-Lymphomen. (Quelle: https://www.gelbe-liste.de/wirkstoffe/Tisagenlecleucel_55482#Anwendung; letzter Aufruf am 8.4.2022)
Axicabtagen Ciloleucel ist zugelassen für die Therapie von
– erwachsenen Patienten mit rezidiviertem oder refraktärem diffus großzelligem B-Zell-Lymphom (DLBCL) und primär mediastinalem großzelligem B-Zell-Lymphom (PMBCL) nach zwei oder mehr systemischen Therapien (Quelle: https://www.gelbe-liste.de/wirkstoffe/Axicabtagen-ciloleucel_55757; letzter Aufruf am 8.4.2022)
Ein drittes Produkt, Lisocabtagen Maraleucel, wurde bisher nur in den USA zugelassen für die Behandlung von erwachsenen Patienten mit verschiedenen Typen von großzelligen B-Zell-Lymphomen. (Quelle: https://www.gelbe-liste.de/onkologie/lisocabtagen-maraleucel-fda-zulassung; letzter Aufruf: 84.2022)
* refraktär: Bestimmte Medikamente sind bei Patienten nicht oder nicht mehr wirksam
** Rezidiv: Krankheitsrückfall
*** systemische Therapie: Behandlung, welche die Wirkung im gesamten Körper entfaltet; das Gegenteil ist eine lokale Therapie, die nur an bestimmten Stellen wirkt.
[1] Zentrum für Krebsregisterdaten. https://www.krebsdaten.de/Krebs/DE/Content/Krebsarten/Morbus%20Hodgkin/morbus%20hodgkin_node.html#:~:text=Das%20Hodgkin%2DLymphom%20ist%20eine,zu%20den%20f%C3%BCnf%20h%C3%A4ufigsten%20Krebsdiagnosen. (letzter Aufruf am 8.4.2022)
[2] Leitlinienprogramm Onkologie: Patientenleitlinie Hodgkin-Lymphom. Abrufbar unter https://www.krebshilfe.de/infomaterial/Patientenleitlinien/Hodgkin-Lymphom_Patientenleitlinie_DeutscheKrebshilfe.pdf (letzter Aufruf am 8.4.2022)
[3] https://www.krebsgesellschaft.de/onko-internetportal/basis-informationen-krebs/krebsarten/non-hodgkin-lymphome/anatomie-und-funktion-des-lymphatischen-systems.html
[4] https://www.krebsinformationsdienst.de/tumorarten/lymphome/index.php
[5] Meier JA et al. The Emerging Role of CAR T Cell Therapy in Relapsed/Refractory Hodgkin Lymphoma. J Pers Med. 2022 Feb 1;12(2):197.
[6] https://www.gpoh.de/kinderkrebsinfo/content/patienten/behandlung/behandlungsmethoden/car_t_zelltherapie/wirkung/index_ger.html (letzter Aufruf am 8.4.2022)
[7] Wang CM et al. Autologous T cells expressing CD30 chimeric antigen receptors for relapsed or refractory Hodgkin lymphoma: An open-label phase I trial. Clin. Cancer Res. 2017; 23: 1156–1166
[8] Ramos C et al. Anti-CD30 CAR-T cell therapy in relapsed and refractory Hodgkin lymphoma. J. Clin. Oncol. 2020; 38: 3794–3804
[9] Grover NS et al. CD30-directed CAR-T cells co-expressing CCR4 in relapsed/refractory Hodgkin lymphoma and CD30+ cutaneous T cell lymphoma. Blood 2021; 138: 742
[10] Voorhees TJ et al. Retrospective Cohort Study Analyzing the Safety and Efficacy of Anti-PD-1 Therapy Following CD30 CAR-T Cell Therapy in Relapsed/Refractory Hodgkin Lymphoma. Blood 2019, 134, 3233

Medizinisches Cannabis in der Onkologie
Kaum ein Fachbereich in der Medizin erlebt eine derartige Innovationsdichte wie die Onkologie. Geforscht wird in alle Richtungen. Neue Erkenntnisse in der Molekularbiologie treffen auf technisches Equipment, das mit einer kaum vorstellbaren Präzision interveniert. Gleichzeitig wird an unterstützenden oder supportiven Therapien geforscht, die zum Beispiel eingesetzt werden, um gravierende Nebenwirkungen wie sie unter anderem bei einer Chemotherapie auftreten können, abzuschwächen.
Spätestens seit medizinisches Cannabis in Deutschland 2017 „legalisiert“ wurde, sind Tetrahydrocannabinol (THC) und Cannabidiol (CBD) – die wichtigsten Cannabinoide und somit Wirkstoffe der Hanfpflanze – auch verstärkt in den Fokus der Wissenschaft geraten. Der Grund:
- THC wirkt unter anderem antiemetisch (Brechreiz-unterdrückend), relaxierend und sedierend.
- Cannabidiol (CBD) hat unter anderem eine anti-psychotische, anxiolytsche (angstlösende), anti-inflammatorische (entzündungshemmende) und spasmolytische (krampflösende) Wirkung.
©iStock / Cavan Images
Wissenschaftlich belastbare Erkenntnisse zu THC- und CBD-Wirkungen liegen bislang für Schmerzen, Spastiken, Übelkeit und Erbrechen durch Zytostatika (Chemotherapie) vor. Als wahrscheinlich gilt eine gute Wirksamkeit bei Appetitlosigkeit, Schizophrenie, Morbus Parkinson, Tourette-Syndrom, Epilepsie, Kopfschmerzen (Migräne) sowie chronisch entzündliche Darmerkrankungen. Alles Eigenschaften beziehungsweise Wirkweisen, die gut in das Behandlungsprofil von an Krebs erkrankten Menschen passen.
Übelkeit und Erbrechen gehören fast immer zu den Nebenwirkungen einer Chemotherapie. Vermutet wird ein Überschuss Serotonin in speziellen Zellen, die in großer Anzahl im Magen-Darm-Trakt zu finden sind.
Der Vagusnerv (Nervus vagus), Hauptnerv des parasympathischen Nervensystem im Verdauungstrakt, hat 5-HT-Rezeptoren oder auch Serotonin-Rezeptoren. Über diese Verbindung könnte das Brechzentrum angeregt werden. Cannabinoide sollen die Serotonin-Rezeptoren blockieren.
Im onkologischen Behandlungs-Alltag wird trotzdem fast ausschließlich auf klassisch-pharmazeutisch produzierte Antiemetika zurückgegriffen.
Mangelernährung bei Krebskranken ist ein häufig unterschätztes Problem. Der Ernährungsmediziner Dr. Matthias Riedl, ärztlicher Leiter des Medicum Hamburg, Europas größtem Zentrum für Ernährungsmedizin und Prävention sowie Adipositas, sagt: „Zurzeit ist es so, dass 30 Prozent der an Krebs erkrankten Menschen bei uns aufgrund einer Mangelernährung regelrecht verhungern. Sie sterben nicht am Krebs. Das ist solide belegt.“
Doch es ist schwierig, ein gesundes Hungergefühl zu entwickeln, wenn ein lebenswichtiges Stoffwechselhormon fehlt. Das Hormon Ghrelin läuft in der Medizin auch unter der Bezeichnung Heißhunger-Hormon. Ghrelin ist die Abkürzung für Growth Hormone Release Inducing. Ghrelin ist in Wachstumsprozessen des Körpers involviert und reguliert das Hunger- und Sättigungsgefühl.
Zum Einsatz kommt das Heißhunger-Hormon im Magen-Darm-Trakt inklusive Bauchspeicheldrüse und wirkt über den Hypothalamus auf das Hungergefühl. Bekommt der Körper über einen längeren Zeitraum nichts zu essen, steigt die Ghrelin-Konzentration im Blut – und löst so den Essensreflex aus.
Wird bei einer Chemotherapie (vor allem mit Cisplatin) vermehrt Serotonin freigesetzt, wird das Heißhunger-Hormon reduziert. Die Folge ist Appetitlosigkeit, obwohl der Magen leer ist. Mangelernährung droht. Die Wirkstoffe von medizinischem Cannabis sind in der Lage, direkt die entsprechenden Rezeptoren des Gehirns zu besetzen und sogar das Sättigungshormon Leptin fernzuhalten. Beim Freizeitkonsum von nicht-medizinischem Cannabis wird das als „Fress-Flash“ bezeichnet – Hunger, obwohl eigentlich nichts mehr reinpasst.
Durchfall gehört zu den häufigsten Nebenwirkungen vieler Krebstherapien wie Chemo- und Strahlentherapie, kann aber auch ein Symptom verschiedener Krebsentitäten wie Lymphome, Darmkrebs und Pankreaskrebs sein. Für ohnehin geschwächte Patienten kann sich langanhaltender Durchfall zu einer lebensbedrohlichen Situation auswachsen. Folgen können eine starke Dehydrierung und Bauchschmerzen sein.
Medizinisches Cannabis hat in medizinischen Studien eine positive Wirkung auf den Verdauungstrakt gezeigt. Der wahrscheinliche Grund für die positive Wirkung: Im gesamten Verdauungstrakt gibt es viele Cannabinoid-Rezeptoren. Diese könnten durch THC und CBD aktiviert werden und entzündungshemmend wirken. Vor allem die CB1-Rezeptoren könnten eine wichtige Rolle spielen.
„Angst, Niedergeschlagenheit und Verzweiflung sind Gefühle, die viele Kranke und ihre Angehörige nach einer Krebsdiagnose empfinden. Angesichts des unsicheren Verlaufs und der tiefgreifenden Lebensveränderungen, die mit der Krankheit und Behandlung verbunden sein können, ist es ratsam, um geeignete psychotherapeutische Unterstützung zu bitten. Depressionen sind bei Krebserkrankungen ein ernstzunehmendes Problem.“
Das schreibt die Deutsche Krebsgesellschaft auf ihrer Website Onko Internetportal. Ob tatsächlich eine Depression vorliegt, müssen die behandelnden Ärzte entscheiden. Für die Diagnose hat die Amerikanische Psychiatrische Vereinigung (APA) eine Checkliste ausgearbeitet. Treffen fünf oder mehr Punkte über einen Zeitraum von zwei Wochen zu, sprichen Mediziner von einer „Major Depression“. Neben einer bedrückten Gemütslage, die von Niedergeschlagenheit über Traurigkeit bis hin zu Hoffnungs- und Mutlosigkeit reichen kann, gibt es weitere typische Anzeichen. Dazu gehören:
– auffallende Ruhelosigkeit oder auffallend verlangsamte Bewegungen
– beeinträchtigte Fähigkeit, Entscheidungen zu treffen
– Energieverlust / Müdigkeit
– Gefühle von Wertlosigkeit
– signifikant verringerte(s) Interesse / Freude an (fast) allen Aktivitäten
– übermäßiges Schlafbedürnis oder Schlaflosigkeit
– Übermäßige / unangemessene Schuldgefühle
– veränderter Appetit (gesteigert oder verringert) / auffallende Gewichtszunahme oder -abnahme
– verringerte Konzentration
– wiederkehrend Todes- / Selbstmordgedanken
CBD-haltige Präparate können wegen ihres stimmungsaufhellenden Effekts Angstzuständen, Panikattacken oder anderen psychischen Belastungen gegensteuern. Die Laune des Betroffenen wird gehoben, Stress verringert und selbst die Schlafqualität verbessert. Aber: Medizinisches Cannabis kann zwar kurzfristig die Stimmung aufhellen, das muss allerdings nicht dauerhaft sein. Eine Therapie mit medizinischem Cannabis muss deswegen unter strenger ärztlicher Kontrolle stattfinden.
Schmerzreduktion ist gerade in der palliativen Onkologie ein zentrales Thema. Besteht therapeutisch keine Chance mehr, eine finale Progression der Krebserkrankung zu stoppen, kommen starke Opiate zum Einsatz, die zwar sehr schnell zu einer Abhängigkeit führen, was aber wegen der Lebenssituation billigend in Kauf genommen wird.
In einem früheren Stadium der Krankheit können die Schmerzen mit nicht abhängig machendem medizinischem Cannabis therapiert werden. Dabei muss allerdings zwischen zwei verschiedenen Arten des Schmerzes unterschieden werden:
1. neuropathische Schmerzen, die durch Schädigungen oder Erkrankungen des Nervensystems auftreten
2. nozizeptive Schmerzen, bei denen die Nervenbahnen nur als Übermittler des Schmerzempfindens dienen
Relativ sicher ist, dass THC bei neuropathischen Schmerzen Linderung verschafft. Denn Dronabinol (aus der Cannabis-Pflanze gewonnenes THC) kann grundsätzlich die Übertragung der Schmerzreize hemmen. Schmerzpatienten erleben objektiv und subjektiv eine Verbesserung der Lebensqualität.
Medizinisches Cannabis kann die Lebensqualität eines Krebspatienten verbessern, indem es Therapie-Nebenwirkungen weniger belastend macht. In der Palliativ-Medizin verschreiben umsichtige Palliativ-Ärzte den Menschen mit sehr schlechter Prognose, medizinisches Cannabis auch dann, wenn eigentlich keine medizinische Indikation vorliegt. Einfach nur, weil die Patienten das wünschen.
Als direkte Behandlungsoption für Primärtumore und deren Metastasen gibt es für medizinisches Cannabis keine seriösen Empfehlungen, weil die Studienlage so dürftig ist, dass sich daraus keine Therapie-Optionen ableiten lassen. Sehr verhalten geforscht wird unter anderem an der Möglichkeit, dass medizinisches Cannabis durch Belegung verschiedener Rezeptoren ein Tumorwachstum stoppen könnte.
Cannabis-Exkurs für Krebs-Betroffene
Die Cannabispflanze wird seit Jahrtausenden als Heil- und Nutzpflanze eingesetzt. Ihr medizinisches Potenzial sitzt vor allem in den Cannabisblüten und den Blüten-nahen Blättern. Man unterscheidet die Pflanzen-Arten Cannabis indica und Cannabis sativa. Der Sativa-Indica-Unterschied besteht zum einen aus Unterschieden in den äußerlichen Merkmalen, zum anderen in unterschiedlichen pharmakologischen Wirkweisen. Einfach heruntergebrochen heißt es, dass die Sativa-Wirkung mehr den Geist, die Indica-Wirkung hingegen mehr den Körper betrifft.
Die Cannabis-Wirkung der verschiedenen Cannabissorten hängt von ihren spezifischen Inhaltsstoffen, genauer von deren Konzentration ab. Haze-Sorten beispielsweise sind für ihren hohen THC-Gehalt bekannt. Neben Cannabinoiden wie THC, CBD und CBG sind noch weitere Inhaltsstoffe relevant: Terpene sind nicht nur maßgeblich verantwortlich für den Geruch und Geschmack der verschiedenen Cannabissorten, sondern beeinflussen auch die Wirkung.
Wenn Cannabis-Ärzte Blüten zum Rauchen verschreiben, empfehlen sie häufig die Nutzung einer speziellen E-Zigarette: Ein Vaporizer ermöglicht es, das medizinische Cannabis kontrolliert bei einer bestimmten Temperatur zu verdampfen und zu inhalieren.
In einer sogenannten Cannabis-Apotheke, also einer auf Cannabis spezialisierten Apotheke, sind neben Blüten auch weitere Cannabis-Präparate und -Produkte erhältlich. Das muss übrigens keine stationäre Apotheke sein, auch eine Online-Apotheke darf sowohl rezeptpflichtiges als auch frei verkäufliches Cannabis vertreiben. Nicht rezeptpflichtig sind alle Präparate und Produkte, die einen THC-Gehalt unter 0,2 Prozent aufweisen. Das kann beispielsweise CBD-Öl oder CBG-Öl sein. Die Cannabisöl-Wirkung bei den Hauptwirkstoffen CBD und CBG ist übrigens ähnlich, aber nicht identisch. Lassen Sie sich bei Interesse von einem Arzt oder Apotheker beraten.

©iStock / LPETTET
Medizinisches Cannabis für Krebs-Patienten gibt es in diesen Arzneiformen
- Nabilon ist ein synthetisches Cannabinoid (THC-Derivat) in Kapselform.
- Dronabinol (Tetrahydrocannabinol, THC) ist in Kapselform oder als ölige Lösung zur oralen Einnahme sowie als Lösung zur Inhalation verfügbar.
- Cannabidiol (CBD) wird aus der Hanfpflanze (Cannabis sativa) gewonnen und wird als ölige Lösung verwendet.
- Nabiximols ist ein Extrakt aus der Hanfpflanze und als Mundspray verfügbar. Es beinhaltet eine 1:1-Kombination von THC und CBD in definierter Menge.
- Medizinisches Cannabis (Medizinalhanf) sind die Blüten der Hanfpflanze. Deren Konzentration an THC und CBD schwankt, je nach eingesetzter Sorte. Es kann etwa als Tee oder zum Zubereiten zur Inhalation nach Verdampfen verschrieben werden.werden.
Was unbedingt beachtet werden muss: Cannabinoid-haltige Fertigarzneimittel sind nicht für alle Patienten geeignet. Zum Beispiel sollten die verschiedenen zugelassenen Arzneimittel nur mit äußerster Vorsicht bei Patienten mit Leber- oder Nierenfunktionsstörungen angewendet

©iStock / Ivan-balvan
Juristische Grundlagen für eine Therapie mit medizinischem Cannabis
Einen Anspruch auf eine möglicherweise sinnvolle Behandlung mit medizinischem Cannabis gibt es nicht. Es bleibt weiterhin dem Arzt überlassen, ob er tatsächlich zum Rezeptblock greift. Die Therapie-Hoheit liegt immer beim behandelnden Arzt – und es gibt bislang nur wenige Ärzte, die bereit sind, medizinisches Cannabis zu verschreiben. Vielfach sind es Vorbehalte und mangelnde Kenntnis, die Ärzte davon abhalten, ein Cannabis-Rezept auszustellen. Im Zweifel greifen sie erfahrungsgemäß eher zu Fertigmedikamenten. Bei Cannabis-Blüten sind die Hürden noch höher.
Krebs-Komplementärmedizin: Nebenwirkungen lindern, Lebensqualität steigern
Erhalten Menschen die Diagnose Krebs und benötigen sie infolgedessen eine Chemotherapie oder andere Behandlungen, ist das ein lebensveränderndes Ereignis. Viele Krebspatienten wollen neben der eigentlichen Therapie auch selbst etwas zu ihrer Heilung beitragen und greifen daher zu sogenannten komplementären Methoden. Den meisten Betroffenen geht es wohl darum, Nebenwirkungen der Krebstherapie zu lindern und die eigene Lebensqualität zu verbessern. Hier setzt die Komplementärmedizin an: Sie beinhaltet Verfahren, die ergänzend zur Schulmedizin eingesetzt werden. Abgegrenzt werden sollte der Begriff von der Alternativmedizin, bei der häufig keine gleichzeitige schulmedizinische Behandlung stattfindet. (Quelle)
2021 wurde erstmals eine Leitlinie zur „Komplementärmedizin in der Behandlung von onkologischen Patienten“ veröffentlicht. In Leitlinien wird das aktuelle medizinische Wissen zu Erkrankungen zusammengefasst. Sie enthalten Empfehlungen, wie Krankheiten festgestellt und behandelt werden sollen, und sie informieren darüber, wie gut eine solche Empfehlung wissenschaftlich belegt ist. Sie geben Ärzten daher eine Orientierungshilfe, sind aber rechtlich nicht verbindlich. (Quelle)
Die Leitlinie zur „Komplementärmedizin in der Behandlung onkologischer Patienten“ zielt darauf ab, die wichtigsten Methoden, Verfahren und Substanzen, die zur komplementären und alternativen Medizin zählen und die Patienten häufig nutzen, zu bewerten. Grundlage für die Bewertung ist die sogenannte „evidenzbasierte Medizin“. Diese stellt aktuelle und wissenschaftlich geprüfte Informationen (aus aussagekräftigen wissenschaftlichen Studien) zu verschiedenen medizinischen Verfahren oder Therapien bereit. Dank der evidenzbasierten Medizin ist es möglich, herauszufinden, welche Vor- und Nachteile eine Behandlung hat oder wann sie einem Patienten nützt oder ob sie sogar schaden kann. (Quelle)

©iStock / 3D_generator
Kernaussagen der medizinischen Leitlinien
Der Krebsinformationsdienst des Deutschen Krebsforschungszentrums schreibt in seinem Informationsblatt über alternative und komplementäre Krebsmedizin. Darin wird unter anderem darauf eingegangen, warum die Krankenkassen viele komplementäre oder alternative Methoden nicht übernehmen und bei welchen Anbietern verschiedener Verfahren Patienten besonders vorsichtig sein sollte.
Herausgeber der Leitlinie ist das Leitlinienprogramm Onkologie der Arbeitsgemeinschaft der Wissenschaftlichen Medizinischen Fachgesellschaften e.V. (AWMF), Deutschen Krebsgesellschaft e.V. (DKG) und Deutschen Krebshilfe (DKH). Verschiedene Fachgesellschaften waren an der Erstellung der Leitlinie beteiligt.
Generell gibt es zur komplementären und alternativen Medizin nur wenig wissenschaftliche Daten, weshalb noch immer großer Forschungsbedarf besteht. Einige Studien deuten aber darauf hin, dass manche Verfahren tatsächlich nützlich sein können – gerade in Bezug auf die Lebensqualität oder bei der Linderung von Symptomen, die durch die Erkrankung selbst oder durch Krebstherapien entstehen. „Sollte“ bedeutet dabei: Empfehlung. „Soll“ bedeutet: starke Empfehlung.
Die Leitlinienautoren empfehlen, Patienten frühestmöglich und im Verlauf wiederholt zur Anwendung von komplementären Methoden zu befragen. Komplementäre Verfahren können die eigentliche Krebstherapie beeinflussen – darauf sollten Betroffene hingewiesen werden. Ärzte sollten weiterhin unseriöse Methoden benennen. Die Aufklärung ist essenziell, denn im Schnitt nutzt circa die Hälfte der Patienten im Verlauf der Erkrankung oder Behandlung mindestens ein komplementäres Verfahren.
Bei der Akupunktur werden Nadeln in definierte Punkte der Körperoberfläche gestochen. Das soll Störungen des Organismus positiv beeinflussen. Die Therapie soll den Qi-Fluss regulieren und somit zur Heilung beitragen. Wissenschaftlich betrachtet ist die Akupunktur wohl eher ein Reizereignis, das Mechanismen der Schmerzhemmung und Regeneration anstößt.
Forscher prüften in Studien, ob eine Akupunktur Schmerzen in Gelenken, die bei Brustkrebspatientinnen von einer bestimmten Therapieform hervorgerufen werden können, verringern kann. Aufgrund der positiven Daten empfehlen die Leitlinienautoren den Einsatz der Akupunktur, um Gelenkschmerzen zu lindern (sollte-Empfehlung). Weitere Daten liegen zur Anwendung der Akupunktur vor, um Tumorschmerzen zu reduzieren. Auch hier gibt es in der Leitlinie eine „sollte“-Empfehlung für den Einsatz.
Tai Chi, oft auch als „Schattenboxen“ bezeichnet, ist eine weltweit praktizierte Bewegungsform, die ursprünglich aus der Selbstverteidigung hervorgegangen ist und die eine Abfolge von Übungen mit langsamen und fließenden Bewegungen beinhaltet. Daneben werden beim Tai Chi auch Atemtechniken sowie kognitive Fähigkeiten integriert.
Qigong zeichnet vereinfachte Bewegungsabläufe und Wiederholungen der Bewegungsroutine aus. Die Techniken von Tai Chi und Qigong überschneiden sich aber zu großen Teilen.
In Studien wurde gezeigt, dass Tai Chi / Qigong bei Fatigue sowie Ein- und Durchschlagstörungen während und nach der onkologischen Therapie helfen kann. Daher sprechen die Leitlinienautoren eine „sollte“-Empfehlung aus.
Yoga gehört in den USA zu den am häufigsten komplementärmedizinisch genutzten Methoden. Auch in Deutschland praktizieren viele Menschen die Haltungen, Übungen und fließenden Bewegungsabfolgen: In einer Umfrage gaben 3,3 Prozent der Befragten an, zurzeit Yoga zu praktizieren, und 15,1 Prozent hatten dies in ihrem Leben bereits getan.
Studien zufolge kann Yoga eine Fatigue (d. h. eine extreme Müdigkeit / Erschöpfung) von Krebspatienten vor und nach onkologischen Behandlungen lindern. Laut der Leitlinie sollte Yoga daher zur Senkung von Fatigue empfohlen werden.
Ein klares Statement gibt es in der Leitlinie zu Sport und Bewegung für onkologische Patienten: Generell soll den Betroffenen empfohlen werden, unter und nach Abschluss der Krebstherapie körperlich aktiv zu sein. Die Leitlinienautoren raten insbesondere dazu, körperliche Inaktivität zu vermeiden. Außerdem sei das Ziel, „mindestens 150 Minuten moderate oder 75 Minuten anstrengende körperliche Aktivität pro Woche so früh wie möglich nach der Diagnose wieder zu erreichen oder aufrechtzuerhalten.“ Mehr Infos: „Krebsrückfall senken: Mit Sport dem Krebs davonlaufen“.
Weitere Empfehlungen:
– Onkologische Patienten sollen zum Erhalt von motorischen Fähigkeiten ein Training mit Ausdauer-, Kraft-, Koordinations- und Beweglichkeitstraining absolvieren.
– Körperliche Aktivität und Sport eignen sich zur Behandlung und Prävention einer krebsspezifischen Fatigue und sollen daher empfohlen werden.
– Gleiches gilt, um die Lebensqualität zu erhalten.
Welche Art des Sports /der Bewegung und welche Intensität geeignet ist, hängt vom jeweiligen Zustand des Patienten, von seiner Belastbarkeit, der körperlichen Bewegungsfreiheit und von seinen Vorlieben ab. Dabei sollte die sportliche Betätigung nicht über die eigene Belastungsgrenze hinausgehen.
In mehreren Abschnitten empfehlen die Leitlinienautoren explizit, auf die Anwendung bestimmter Verfahren, Vitamine oder Maßnahmen zu verzichten. Auch eignen sich die meisten komplementären Maßnahmen nicht, um die Lebenszeit zu verlängern oder das Risiko zu senken, dass der Krebs zurückkommt. Eine explizite Warnung sprechen die Experten für Amygdalin / Laetrile aus. Diese oft auch als „Vitamin B17“ bezeichnete Pflanzenverbindung ist in den Kernen vieler Früchte enthalten – unter anderem in Aprikosenkernen. Die Substanz wird über mehrere Zwischenstufen in Benzaldehyd und Cyanid (Blausäure) umgewandelt, das möglicherweise giftig wirkt. Auch der Krebsinformationsdienst des Deutschen Krebsforschungszentrums warnt vor der Einnahme von Aprikosenkernen: Blausäure kann schwere Vergiftungen verursachen, oft begleitet von Kopfschmerzen, Übelkeit und Erbrechen. In schlimmsten Fall drohen Atemnot und Tod.
In Studien rief Amygdalin teils schwere und potenziell lebensbedrohliche Nebenwirkungen hervor. Zudem gibt es keinerlei Hinweise auf Effekte, die sich positiv auf eine Tumorerkrankung auswirken könnten. Amygdalin, Laetrile oder Aprikosenkerne sollen daher nicht empfohlen werden.
Die Leitlinien-Autoren sprechen eine Reihe weiterer soll- / sollte-Empfehlungen aus. Dazu gehören:
Onkologischen Patienten mit verminderter Knochenstabilität, zum Beispiel durch Knochenmetastasen oder Osteoporose, soll im Fall einer Verletzungsgefahr von einer Chirotherapie oder Osteopathie mit manipulativen Techniken oder Impulstechniken abgeraten werden.
Eine ketogene Ernährung (d. h. eine kohlenhydratarme Kost) soll nicht bei normalgewichtigen und untergewichtigen Patienten empfohlen werden.
Um Mangelzustände zu erkennen, sollten bei onkologischen Patienten die Vitamin D-Spiegel gemessen werden.
Krebs-Komplementärmedizin: Übersicht über die Leitlinien-Empfehlungen
Die folgende Tabelle ist in abgewandelter Form aus der Leitlinie entnommen. Sie gibt einen Überblick über evidenzbasierte, komplementäre Therapien zur Verbesserung von Symptomen und Lebensqualität von Erkrankten unter oder nach einer Krebstherapie. Achtung: Die Methoden wurden nur bei bestimmten Patienten (z. B. Brust- oder Prostatakrebs), zu bestimmten Zeitpunkten (z. B. vor oder nach einer Krebstherapie) und bei bestimmten Behandlungen (z. B. Bestrahlung oder Chemotherapie) untersucht. In der Tabelle wird aus Gründen der Übersichtlichkeit teilweise auf diese Angaben verzichtet.
Ein Beispiel: In einer Studie wurden Angst / Ängstlichkeit von Brustkrebspatientinnen nach Abschluss einer Chemotherapie oder unter bestimmten anderen Medikamenten durch Akupunktur verringert. Die vollständigen Informationen, welches Verfahren, wann unterstützend wirken kann, finden Interessierte in der Leitlinie ab Seite 19.
Sind keine Angaben zu einer bestimmten Patientengruppe gemacht, gilt die Empfehlung für alle onkologischen Betroffenen. Für manche Verfahren gibt es eine konkrete Empfehlung, diese bei bestimmten Symptomen einzusetzen.
| Symptom / Ziel | soll / sollte eingesetzt werden | kann (muss aber nicht) bestimmten Patienten helfen – Empfehlung offen | soll / sollte nicht eingesetzt werden | keine ausreichenden Datenlage |
| Angst / Ängstlichkeit | – Akupunktur (Brustkrebs) – Mindfulness-based Stress Reduction (Brustkrebs) – Meditation (Brustkrebs und Leukämie) – Yoga (Kolorektalkarzinom) | Bioenergiefeld-Therapien | – Kunsttherapie – Schwedische Massage | |
| Appetit | Carnitin | |||
| Dermatitis (entzündliche Hautreaktion) | Aloe Vera-haltige Cremes, Lotions oder Aloe Vera Gele zur Vorbeugung einer Radiodermatitis (soll nicht) | – Boswellia serrata (auf die Haut aufgetragen) gegen strahleninduzierte Dermatitis – Zinksupplementation zur Vorbeugung | ||
| Depressivität (nicht im Sinne einer diagnostizierten Depression zu verstehen) | – Akupunktur (Brustkrebs) – Mindfulness-based Stress Reduction -Meditation – Tai Chi / Qigong – Yoga (Kolorektalkarzinom) | Bioenergiefeld-Therapien | – Kunsttherapie – Schwedische Massage | |
| Distress | Schwedische Massage | |||
| Geschmacksstörung | Zink zur Prävention | |||
| Ein- und Durchschlafstörungen | Tai Chi / Qigong (sollte), während und nach Abschluss von Chemo- / Radiotherapie | – Akupunktur – Mindfulness-based Stress Reduction – Yoga (Brustkrebs) – Anthroposophische Komplexbehandlung (Überlebende nach Brustkrebs) | – Baldrian – Bryophyllum pinnatum – Schwedische Massage – Meditation | |
| Entspannung | Schwedische Massage | |||
| Erektile Dysfunktion | Yoga | |||
| Fatigue | – Körperliche Aktivität und Sport (soll) – Tai Chi / Qigong (sollte) – Yoga (sollte) | – Akupunktur – Akupressur – Ginseng – (ärztlich geleitetes), individualisiertes, multimodales komplementärmedizinisches Therapieangebot (Brustkrebs) – Mindfulness-based Stress Reduction – Anthroposophische Komplexbehandlung (Überlebende nach Brustkrebs) | – Bioenergiefeld-Therapien – Guarana-trockenextrakt | – Bryophyllum pinnatum (Phytotherapeutische Dosierung) – Carnitin – Kunsttherapie – Meditation – Schwedische Massage – Zink (Prävention) |
| Hand-Fuß-Syndrom | Vitamin B6 | |||
| Ileus (Darmverschluss) | Akupunktur (Kolonkarzinom) | |||
| Kognitive Beeinträchtigung | – Akupunktur (Brustkrebs) – Mindfulness-based Stress Reduction (Brustkrebs) – Yoga (Brustkrebs) | – Ginkgo biloba (Brustkrebs) – Meditation | ||
| Lebensqualität | Körperliche Aktivität und Sport (soll) | – Akupunktur – (ärztlich geleitetes), individualisiertes, multimodales komplementärmedizinisches Therapieangebot (Brustkrebs – Klassische Homöopathie – Mindfulness-based Stress Reduction – Meditation (Brustkrebs) – Subkutane (unter die Haut) Gabe von Mistelgesamtextrakt enthaltenden Arzneimitteln (solide Tumoren) – Tai Chi / Qigong – Yoga (Brustkrebs) | – Vitamin E und Beta-Carotin (soll nicht) (Kopf-Hals-Tumoren) – Bioenergiefeld-Therapie · Ketogene Diät (Ovarial-/Endometriumkarzinom) – Vitamin B12 und Folsäure (Lungenkrebs und Mesotheliom) | – Anthroposophische Behandlungen (z. B. Einnahme natürlicher Präparate, Kunsttherapie, Exposition Bestrahlung mit buntem Licht, Musik- und Sprachtherapie, Heileurythmie, Diät, therapeutische Massage, Hydrotherapie und teilweise auch Misteltherapie) – Carnitin – Epigallocatechingallat (grüner Tee) – Heilpilze – in Deutschland registrierte homöopathische Einzelmittel / Komplexmittel – schwedische Massagen |
| Lymphödem | Yoga | |||
| Menopausale Symptome | – Akupunktur – Cimicifuga racemosa (Traubensilberkerze) (Brustkrebs) – Mindfulness-based Stress Reduction (Brustkrebs oder andere gynäkologische Tumoren) – Yoga (Brustkrebs) | – Isoflavone (Soja, soll nicht) (Brustkrebs) – Vitamin E (soll nicht) (Brustkrebs) | ||
| Mukositis (Entzündung der Mundschleimhaut) | – Natriumselenit (Gebärmutter,- Gebärmutterhalskrebs, fortgeschrittene Kopf-Hals-Tumoren) – Zink (Supplementation) | – Vitamin E (soll nicht) (Kopf-Hals-Tumoren) – Vitamin E (sollte nicht, andere onkologische Patienten) – Zink (soll nicht) | – Aloe vera-haltige Mundspülungen – Aloe Vera-haltige Rektalsalbe – Aloe Vera-Säfte zur Prophylaxe – Kurkuma bei topischer (auf die Haut aufgetragen) Applikation (Kopf-Hals-Tumoren) – Selenit (akute lymphatische oder myeloische Leukämie) | |
| Nebenwirkungen der Androgendeprivation / Androgensuppression* | Isoflavone (Prostatakarzinom) | |||
| Neutropenie** | – Vitamin B12 und Folsäure (Lungenkarzinom und Mesotheliom im fortgeschrittenen Stadium) | |||
| Entzündung der Speiseröhre | Zink zur Prävention | |||
| Störungen der Innenohr-Funktion | Vitamin E (soll nicht) | |||
| Schädigung peripherer Nerven (periphere Polyneuropathie) | – Carnitin (soll nicht) – Vitamin E (soll nicht) | – Kombination aus Vitamin B1 und Vitamin B6 – Vitamin B12 (isolierte Gabe) | ||
| Rachenentzündung | Zink zur Prävention durch Supplementation | |||
| Schmerz | Akupunktur (sollte) (Brustkrebs und andere onkologische Patienten) | – Akupunktur (Patienten mit durch eine Chemotherapie verursachten peripheren neuropathischen Schmerzen) – Elektroakupunktur (Patienten mit Prostataentfernung) – Elektroakupunktur (Patienten während Hirntumoroperationen) – (ärztlich geleitet) individualisiertes, multimodales komplementärmedizinisches Therapieangebot (Brustkrebs) – Ohr-Akupressur (Tumorschmerzen) | Bioenergiefeld-Therapien | Schwedische Massage |
| Schulterbeweglichkeit | Yoga | |||
| Stimmung / Affekt | Schwedische Massage | |||
| Stress | – achtsamkeitsbasierte Atemtechnik – Mindfulness-based Stress Reduction | – Schwedische Massage – Yoga | ||
| Übelkeit / Erbreachen | – Akupressur (Neiguan, PC6) – Akupunktur (zusätzlich zu einer Brechreiz-lindernden Therapie) – Ingwer | Bioenergiefeld-Therapien | – Schwedische Massage – Yoga | |
| Wohlbefinden | Schwedische Massage | |||
| Wundheilung | Epigallocatechingallat (grüner Tee) | |||
| Mundtrockenheit | Akupunktur | Kombination von Vitamin C und Vitamin E (Kopf-Hals-Tumoren) | Zink | |
| Hirnödem | Boswellia serrata (Hirntumoren) |
FAQ
Entartete Zellen vermehren sich unkontrolliert und zerstören dabei gesundes Gewebe. Über Blut- und Lymphbahnen können diese malignen Zellen in den ganzen Körper streuen und Metastasen bilden. 
@iStock / Dr_Microbe
Gemessen an der 10-Jahres-Überlebensrate ist der Mesotheliom – ein seltener Weichteiltumor, der fast nur Männer im hohen Alter befällt – mit deutlich unter 10 Prozent die gefährlichste Krebsart. Gefolgt von Pankreaskrebs mit ebenfalls unter 10 Prozent, Leber- und Lungenkrebs folgen mit unter 15 Prozent.
Nicht-melanotischer Hautkrebs (heller Hautkrebs), Hodenkrebs, das maligne Melanom (schwarzer Hautkrebs) und Schilddrüsenkrebs haben die geringste Mortalitätsrate und damit höchste 10-Jahres-Überlebensrate (mehr als 90 Prozent). Mit mehr als 80 Prozent gehören auch Prostata- und Brustkrebs zu den Krebsentitäten mit der besten Überlebenschance.
Quelle: https://www.krebsdaten.de/Krebs/DE/Content/Krebsarten/Krebs_gesamt/krebs_gesamt_node.html
@iStock / Marcelo Ricardo Daros
Die 10 Krebsarten mit der höchsten Mortalitätsrate:
– Mesotheliom
– Bauchspeicheldrüse
– Leber
– Lunge
– Zentrales Nervensystem
– Gallenblase und Gallenwege
– Speiseröhre
– Magen
– Eierstöcke
– Multiples Myelom
Quelle: https://www.krebsdaten.de/Krebs/DE/Content/Krebsarten/Krebs_gesamt/krebs_gesamt_node.html
@iStock / da-kuk
Ob eine Krebserkrankung tödlich verläuft, hängt entscheidend von der Art des Krebses und dem Zeitpunkt seiner Entdeckung ab. Grundsätzlich gilt: Je früher ein Tumor entdeckt wird, umso höher ist die Heilungschance. Weil einige Tumoren, wie z. B. Pankreas- oder Bauchspeicheldrüsen oft lange symptomlos verlaufen, werden sie oft erst spät oder nur per Zufall entdeckt. Oft haben sich dann schon Metastasen gebildet (die eine Heilung deutlich erschweren), oder der Krebs kann aufgrund seiner schwierigen Position schlecht entfernt werden.
Prostatakrebs, der erst im Alter jenseits der 70 entdeckt wird, nicht sehr aggressiv und die Vorsteherdrüse noch nicht verlassen hat, verläuft in weniger als einem Prozent der Fälle tödlich. 
@iStock / Design Cells
Krebs ist eine bösartige Störung des Zellwachstum. In der Medizin wird das als Neoplasie oder Malignom bezeichnet. Weil die mutierten Zellen sich den Wachstumssignalen entziehen, vermehren sie sich unkontrolliert und zerstören dabei gesundes Gewebe.
Besonders heimtückisch ist die Krankheit, weil Krebszellen sich vor dem Immunsystem tarnen und deswegen ungestört weiterwachsen können. Eine Selbstheilung des Körpers ist deswegen fast ausgeschlossen.
Darüber hinaus hat jeder einzelne Geschwulst – Tumoren werden in der Medizin nicht als Geschwür bezeichnet – eine ganz individuelle Genetik, die bei keinem Menschen gleich ist. Das macht ihre Behandlung so schwer.
@iStock / howtogoto
Krebs wird heute praktisch immer mit einer Kombitherapie aus verschiedenen Modulen behandelt. Die drei klassischen Säulen einer Krebsbehandlung sind:
– Operation
– Chemotherapie
– Bestrahlung
Bei der Operation wird das bösartige Gewebe chirurgisch entfernt. Oft wird vor dem Eingriff versucht, den Tumor mit einer Chemotherapie oder Bestrahlung zu verkleinern. Ist der Tumor schon sehr groß, kann es sinnvoll sein, wenn der operative Eingriff vor weiteren Therapie-Modulen erfolgt.
Kaum eine andere Fachrichtung der Medizin erlebt mehr Innovationen als die Onkologie. Moderne Therapien arbeiten wie beim Brustkrebs mit Hormonen. Große Hoffnungen setzt die Krebsforschung auf immer präzisere Immuntherapien (z. B. Car-T-Zellen-Therapie), die alle im Grunde darauf basieren, die getarnten Krebszellen für das Immunsystem sichtbar zu machen. 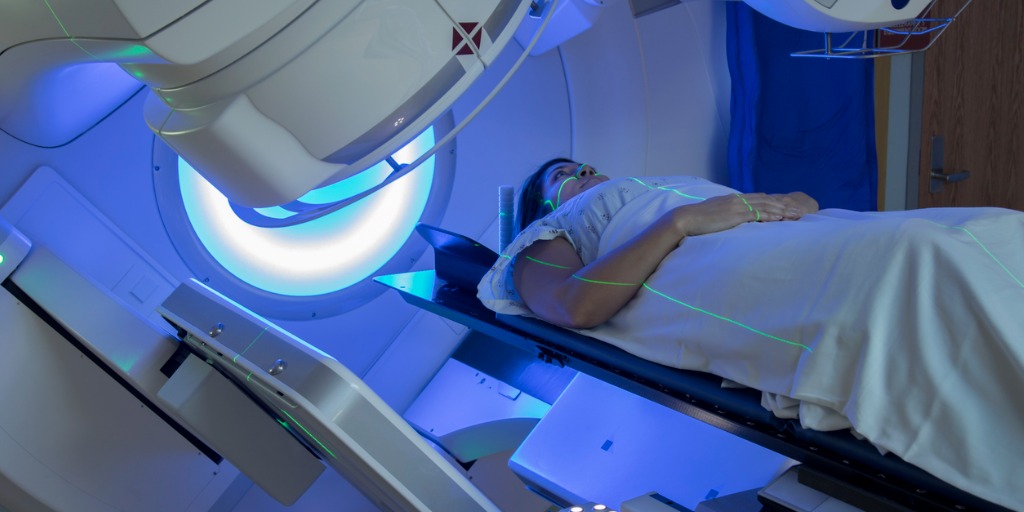
@iStock / FatCamera
Wird Pankreas- oder Bauchspeicheldrüsenkrebs diagnostiziert, ist das fast immer m mit einer sehr schlechten Prognose verbunden, weil der Krebs schon weit fortgeschritten ist. Abgesehen vom Mesotheliom, einem seltenen Weichteiltumor, haben Menschen mit Pankreaskarzinomen mit etwa neun Prozent die schlechteste 10-Jahre-Überlebensrate der weit verbreiteten Krebsarten.
Als eine der aggressivsten Krebsarten gilt das Glioblastom. Etwa 2.500 Menschen jährlich erkranken in Deutschland an diesem Hirntumor. Glioblastome wachsen rasend schnell, verdoppeln sich im Schnitt alle 50 Tage. Glioblastome habe nur eine 5-Jahres-Überlebensrate von etwa 5 Prozent. Die meisten Patienten sterben im Schnitt 15 Monate nach der Diagnose.
Quelle: https://www.focus.de/gesundheit/ratgeber/krebs/krebs-die-5-aggressivsten-arten-und-wie-sie-ihr-risiko-fast-halbieren-koennen_id_11228080.html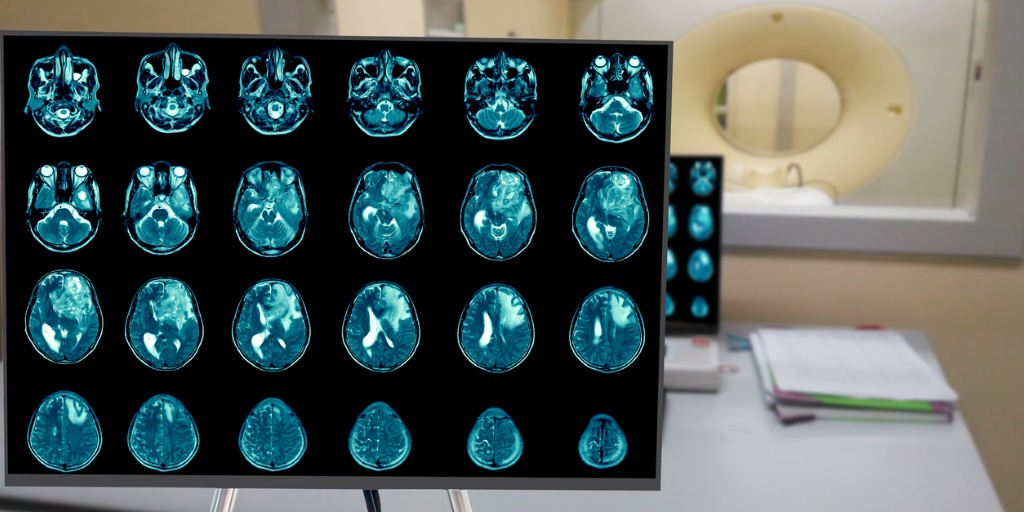
@iStock / Tonpor Kasa
Der Name Krebs geht auf den antiken griechischen Arzt und Lehrer Hippokrates zurück. Er hatte bei Brusttumoren seiner Patienten eine entfernte Ähnlichkeit mit Krebsbeinen entdeckt, sowohl wie sie sich ausbreiteten, aber auch, weil Geschwülste im Vergleich zum umliegenden Gewebe relativ hart sind. Damit gab er der Krankheit den Namen: Karkinos – Krebs.
Krebs muss aber nicht aussehen wie Meeresfrüchte. Entscheidend ist, wo sich die Krebsgeschwulste bilden und in welchem Entwicklungsstadium sie sind. Auffallend ist aber, dass sich maligne Tumore fast immer durch eine unruhige Struktur auszeichnen. 
@iStock / koto_feja
Krebs hat zwei Eigenschaften, die ihn für den Körper unkontrollierbar machen:
1. Krebs wächst ohne Limit und ohne auf natürliche Wachstumssignale zu reagieren. Dabei zerstört er gesundes Gewebe.
2. Krebs ist für das Immunsystem unsichtbar. Deswegen werden Krebszellen nicht attackiert.
Eine Selbstheilung des Körpers ist deswegen so gut wie ausgeschlossen. 
@iStock / Design Cells
Das hängt maßgeblich von zwei Faktoren ab:
1. In welchem Entwicklungsstadium wurde der Krebs entdeckt?
2. Welche Art von Krebs wurde diagnostiziert?
Die besten 10-Jahres-Überlebensraten haben heller Hautkrebs (nicht-melanotischer Hautkrebs), Hodenkrebs, das maligne Melanom (schwarzer Hautkrebs) und Schilddrüsenkrebs: mehr als 90 Prozent.
Prostatakrebs und Brustkrebs gehören mit mehr als 80 Prozent ebenfalls noch zu Krebsarten mit guter Prognose.
Gebärmutter, Niere, Harnblase und Non-Hodgkin-Lymphome liegen zwischen 60 und 80 Prozent. Zwischen 40 und 60 Prozent sind es bei Darmkrebs, Leukämien und Harnblasenkrebs. Tumoren von Eierstöcken, Magen und Speiseröhre haben mit 20 bis 40 Prozent eine deutlich schlechtere Prognose. Bei Lunge, Leber und Bauchspeicheldrüse liegt sie sogar unter 20 Prozent.
Quelle: https://www.krebsdaten.de/Krebs/DE/Content/Krebsarten/Krebs_gesamt/krebs_gesamt_node.html 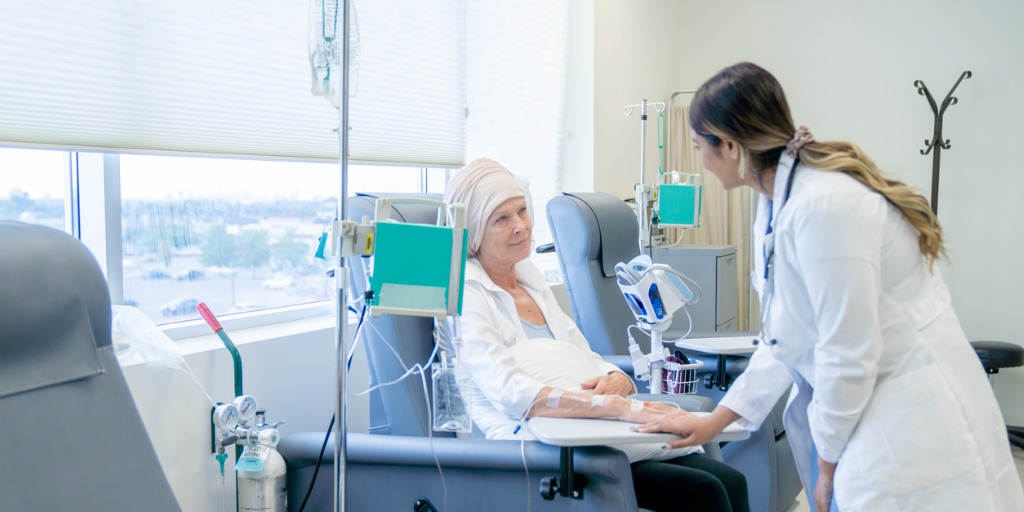
@iStock / FatCamera
Krebs kann ganz verschiedene Ursachen haben, entscheidend ist, sie haben dazu geführt, dass Zellen mutieren und sich unkontrolliert teilen.
Mutationen entstehen unter anderem ganz natürlich als Alterungsprozesse, weswegen die Krebsanfälligkeit im hohen Alter deutlich steigt. Auslöser können aber auch äußere Umweltgifte wie Alkohol, Nikotin, Zucker, Junkfood, Industrie-Emissionen sein. 
@iStock / peterschreiber.media
Die Medizin geht sehr vorsichtig mit dem Wort Heilung in Zusammenhang mit allen Krebsarten um, spricht lieber von einer chronischen Krankheit. Grundsätzlich gilt – und besonders für das Mammakarzinom: Gab es nach zehn Jahren keinen Rückfall, ist die Wahrscheinlichkeit sehr hoch, dass noch Rezidive entstehen. 
@iStock / Cecilie_Arcurs
Die Medizin spricht bei Krebs von einer chronischen Krankheit, die Patienten ein Leben lang begleitet. Patienten gelten aber als geheilt, wenn fünf Jahre nach der Therapie keine Rezidive aufgetreten sind. Das sind in Deutschland zurzeit etwa vier Millionen Menschen.
Immer neue Therapien und Therapieansätze und eine präzisere Diagnostik in der modernen Onkologie verbessern die Überlebenschancen von Krebspatienten deutlich. Trotzdem kann eine Krebsbehandlung auch dauerhafte Gesundheitsfolgen haben.
Quelle: https://www.krebsgesellschaft.de/onko-internetportal/basis-informationen-krebs/leben-mit-krebs/alltag-mit-krebs/langzeitueberleben-nach-krebs-wie-lange-ist-ein-k.html
@iStock / nd3000
Generell gilt CBD als sicher uEs gibt jedes Jahr neue Therapieansätze. Große Hoffnung setzt die onkologische Forschung auf neuartige Immuntherapien, wie die 2018 neu zugelassene Car-T-Zellen-Therapie. Sie zielen alle darauf ab, die bösartigen Zellen für das Immunsystem sichtbar zu machen. Damit will die Medizin das erreichen, was der menschliche Körper bisher nicht kann: Krebs aus eigener Kraft in die Schranken zu weisen. Sollte das gelingen, wäre das Immunsystem nach der Therapie dazu in der Lage, alle Krebszellen im Körper aufzuspüren und die entsprechenden Maßnahmen einzuleiten.
Aktuell erforscht wird unter anderem die Wirkung einer mRNA-Vakzinierung gegen Krebs, die ähnlich funktioniert wie die Corona-Impfung, allerdings für jeden Patienten individuell hergestellt werden muss. 
@iStock / Kanjana Jorruang
Die Lebenserwartung hängt entscheidend von der Art des Tumors und natürlich vom Lebensalter des Patienten ab. Eine akute lymphatische Leukämie (ALL), an der hauptsächlich Kinder erkranken, kann unbehandelt innerhalb von wenigen Wochen zum Tod führen.
Im höheren Alter entdeckter Prostatakrebs bei Männern dagegen muss nicht zwingend behandelt, sollte aber regelmäßig kontrolliert werden.
Quelle: https://www.kompetenznetz-leukaemie.de/content/patienten/leukaemien/all/ 
@iStock / luismmolina
Die Medizin spricht bei Krebs von einer chronischen Krankheit, die Patienten ein Leben lang begleitet. Patienten gelten aber als geheilt, wenn fünf Jahre nach der Therapie keine Rezidive aufgetreten sind. Das sind in Deutschland zurzeit etwa vier Millionen Menschen.
Immer neue Therapien und Therapieansätze und eine präzisere Diagnostik in der modernen Onkologie verbessern die Überlebenschancen von Krebspatienten deutlich. Trotzdem kann eine Krebsbehandlung auch dauerhafte Gesundheitsfolgen haben.
Quelle: https://www.krebsgesellschaft.de/onko-internetportal/basis-informationen-krebs/leben-mit-krebs/alltag-mit-krebs/langzeitueberleben-nach-krebs-wie-lange-ist-ein-k.html 
@iStock / dusanpetkovic
Der Verlauf einer Knochenkrebs-Erkrankung wird in vier Krebs-Stadien unterteilt. Im Knochenkrebs-Endstadium (Stadium IV) sind wir in Stufe III jeglicher Grad der Bösartigkeit und jede Tumorgröße möglich. Bei der Metastasierung wird unterschieden in:
• Stadium IV: Möglicher Befall der Lymphknoten und Metastasen außerhalb der Lunge.
• Stadium IVA: Lymphknoten sind nicht befallen, aber Metastasen in der Lunge.
• Stadium IVB: Lymphknoten in der Nähe des Tumors sind betroffen. Außerdem gibt es Metastasen in der Lunge und / oder anderen Organen. 
@iStock / Gerasimov174
Der Knackpunkt ist das Erbgut. In den Trägern der Erbanlagen, den Genen, sind irreparable Schäden entstanden. Betroffen sind drei Gen-Gruppen:
– Onkogene
– Tumorsuppressor-Gene
– Reparaturgene
In gesunden Zellen funktioniert das so: Die Onkogene unterstützen das Wachstum der Zelle, die Tumorsuppressor-Gene verhindern es. Kommt es zu Problemen durch Mutationen, greifen die Reparaturgene ein und beheben den Schaden. Dieser Mechanismus ist beim Krebs gestört. Die Zellen wachsen ungebremst.
Die Gründe für die gefährlichen Mutationen sind in der Mehrzahl exogener Natur, das heißt sie kommen von außen. Zigaretten, Alkohol, Zucker, starkes Sonnenlicht oder Infektionen mit Krankheitserregern wie humanen Papillomaviren.
Quelle: https://www.krebsgesellschaft.de/onko-internetportal/basis-informationen-krebs/basis-informationen-krebs-allgemeine-informationen/wie-krebs-entsteht.html 
@iStock / elvanegra
In frühen Stadien der Erkrankung macht Leberkrebs nur wenige bis gar keine Beschwerden. Doch im weiteren Verlauf der Krebserkrankung die eingeschränkte bis hin zur verlorenen Funktion der Leber das größte Problem. Kann die Leber keine lebenswichtigen Stoffwechselprodukte mehr liefern und den Körper durch Ausscheidung aller Abfallprodukte nicht mehr entgiften, kommt es zu deutlichen Symptomen:
• Wasser im Bauch / Bauchumfangszunahme
• juckende oder brennende Haut
• Gewichtsverlust
• Appetitlosigkeit
• Druckschmerz im rechten Oberbauch
• Gelbfärbung der Haut 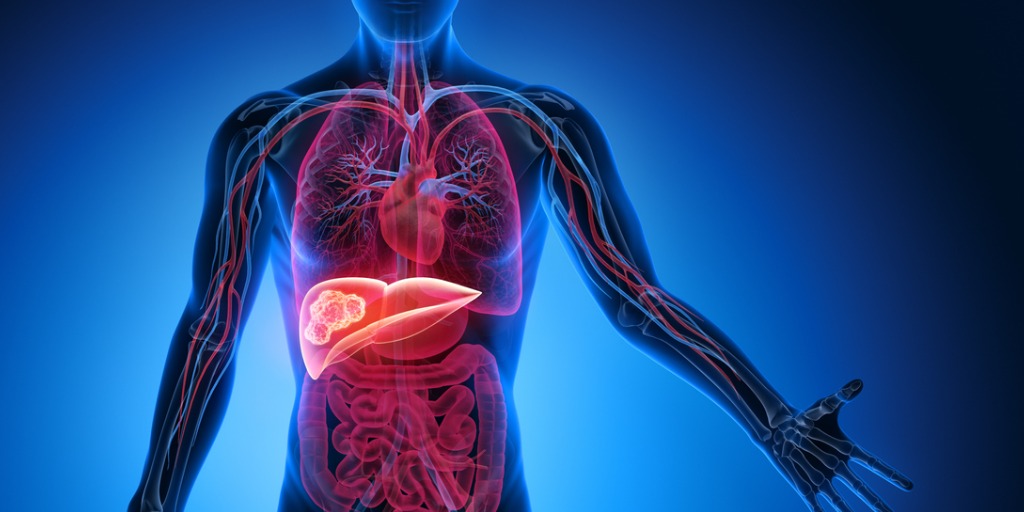
@iStock / peterschreiber.media
Die wichtigsten Krebstherapien:
– Operation bei Krebs
– Strahlentherapie bei Krebs
– Chemotherapie
– zielgerichtete Krebstherapien (targeted therapies)
– Stammzelltransplantation
– Hyperthermie-Behandlung bei Krebs
– Komplementäre Therapie bei Krebs
– Immunonkologie
Quelle: https://www.krebsgesellschaft.de/basis-informationen-krebs/therapieformen.html 
@iStock / whyframestudio
Krebsüberlebende klagen am häufigsten über:
– Erschöpfung
– Schmerzen
– Schlafstörungen
– Ängste
– Sorgen
– Bewegungseinschränkungen
– Polyneuropathie (PNP)
Unterschieden wird zwischen Langzeitfolgen und Spätfolgen. Während Langzeitfolgen fortwährend seit Ende der Therapie andauern (z. B. Polyneuropathie, Fatigue, Erkrankungen des Verdauungstraktes, eingeschränkte Körperfunktionalität durch Amputationen, kognitive Einschränkungen á la Chemobrain), treten Spätfolgen oft erst mit jahrelanger Verzögerung auf. Beispiele für Krebsspätfolgen sind Herzkrankheiten und strahlenbedingte Knochenbrüche.
Quelle: https://www.krebsgesellschaft.de/onko-internetportal/basis-informationen-krebs/leben-mit-krebs/alltag-mit-krebs/langzeitueberleben-nach-krebs-wie-lange-ist-ein-k.html 
@iStock / Chinnapong
Bei einer Chemotherapie werden dem Patienten Medikamente verabreicht, die Zellwachstum und Zellteilung verhindern sollen. Diese Arzneimittel werden als Zytostatika bezeichnet, was so viel wie Zell-Hemmer bedeutet. Zytostatika sind Zellgifte, die so designt wurden, dass sie speziell sich schnell teilende, also schnell wachsende Zellen angreifen. Krebszellen wachsen sehr schnell.
Weil Chemotherapeutika sich im ganzen Körper verteilen, ist es eine systemische Therapie. So werden im Idealfall auch mutierte Zellen gestoppt, die gestreut wurden. Weil Zytostatika auch andere schnell wachsende Zellen attackieren, sind fast immer auch Haarwurzeln betroffen.
Eine regionale oder lokale Chemotherapie wird zum Beispiel bei der Spülung einer Körperhöhle mit einem Zell-Hemmer eingesetzt. Bei Hauttumoren kann das Zellgift lokal über eine Salbe verabreicht werden.
Quelle: https://www.krebsinformationsdienst.de/behandlung/chemotherapie/durchfuehrung.php 
@iStock / fluxfoto
Hippokrates (460 bis 370 v. Chr.), der berühmteste Arzt der Antike und Gottvater der Medizin nannte die rätselhaften Geschwulste Karkinos. Das ist das griechische Wort für Krebs. Die Bezeichnung rührt daher, dass sich gerade Brusttumoren ausdehnen wie die Beine eines Krebses. 
@iStock / luismmolina
Bösartige Geschwulste sind das Ergebnis einer Mutation in den Genen von Zellen. Maligne Zellen können ihr Wachstum nicht mehr regulieren und teilen sich unkontrolliert. 
@iStock / koto_feja
Krebszellen nutzen im Körper zwei Verbreitungswege:
– Lymphogene Metastasierung (über die Lymphbahnen)
– Hämatogene Metastasierung (über das Blut)
Finden die malignen Zellen an anderer Stelle des Körpers geeignete Wachstumsbedingungen, kann so ein sekundärer Tumor, eine Metastase entstehen. Sind die Bedingungen nicht geeignet, sterben die Tumorzellen ab.
Metastasen bilden sich besonders häufig in der Lunge, der Leber und den Knochen. Bei den Knochen besonders betroffen: Wirbelsäule, Becken, Oberschenkel und Oberarme, Rippen und Schädel.
Hände, Füße, Herz, Milz und Nieren sind dagegen fast nie von Metastasen befallen. 
@iStock / imaginima
Etwa 300 verschiedene Krebsarten (Entitäten) sind bekannt. Die Begriffe Krebs, Tumor und Geschwulst (nicht Geschwür) sind Oberbegriffe für alle Krebserkrankungen. Bei den bösartigen Tumoren unterscheidet die Medizin zwischen Karzinomen, Sarkomen und Blastomen.
Karzinome sind die häufigste Krebsart. 80 Prozent der Krebskranken in Deutschland haben ein Karzinom. Karzinome entstehen im Deckgewebe der Haut, der Schleimhaut und des Drüsengewebes. Lungenkrebs heißt medizinisch deswegen zum Beispiel auch Bronchialkarzinom.
Fettgewebe, Sehnen, Muskeln, Knochen oder Knorpel sind der Entstehungsort von Sarkomen. Knochenkrebs heißt zum Beispiel medizinisch korrekt Osteosarkom.
Bei der Gewebe- und Organentwicklung eines Menschen können Zellen zu Blastomen mutieren. Wann diese bösartigen Zellen zu einem Problem werden, hängt von der Art des Blastoms ab. Neuroblastime sind zum Beispiel eine Krebsart, die hauptsächlich bei Kindern auftritt.
Quelle: https://www.krebsinformationsdienst.de/tumorarten/krebs-tumor-metastasen-definition.php 
@iStock / DivVector
Krebsdiagnosen lösen bei fast allen Betroffenen eine existenzielle Lebenskrise aus. Es gibt aber keine wissenschaftlich einheitliche Antwort auf die Frage, welchen Einfluss die Krankheit auf die Psyche hat. Viele Krebspatienten fragen sich „Warum ich?“. Rückt diese Frage in den Mittelpunkt des Denkens, kann sie zu Depressionen führen. Lebenswille und -mut brechen.
Quelle: https://www.uniklinikum-leipzig.de/einrichtungen/frauenheilkunde/Freigegebene%20Dokumente/Patientenseminar_Brustzentrum_06%2002%2019_Peuker.pdf 
@iStock / ljubaphoto
Ergebnis einer repräsentiven Umfrage: 61 Prozent der Deutschen glauben, dass Krebs durch psychischen Stress verursacht werden kann. Die Wissenschaft geht allerdings davon aus, dass es keinen Zusammenhang zwischen psychosozialen Faktoren und der Entstehung von Krebs gibt. Aber eine psychische Belastungssituation kann Gesundheitsverhalten und den Lebensstil (wenig Sport, Alkohol, Nikotin) negativ beeinflussen. Das wiederum ist relevant für die Entstehung von Krebs.
Quelle: https://www.uniklinikum-leipzig.de/einrichtungen/frauenheilkunde/Freigegebene%20Dokumente/Patientenseminar_Brustzentrum_06%2002%2019_Peuker.pdf 
@iStock / PeopleImages
Aufgrund der Schwere der Krankheit kann eine Krebserkrankung tiefgreifende körperliche und psychische Auswirkungen auf den Menschen haben. Die erste gravierende Belastung ist die Krebsdiagnose, die das Urvertrauen an den eigenen Körper schwer belasten und Depressionen verursachen kann.
Die eigentliche Krebstherapie kann den Körper ebenfalls nachhaltig in Mitleidenschaft ziehen. So sterben bei einer Chemotherapie häufig auch unwiederbringlich die Nervenenden in den Füßen (Polyneuropathie oder kurz PN). Andere Veränderungen entstehen durch Amputationen, geschädigte Organe etc. 
@iStock / fedrelena
Bekannt sind etwa 300 verschiedene Krebsarten, von den die weitaus meisten aber zu den seltenen Krankheiten gehören. Bösartigen Krebsentitäten werden, je nach Entstehungsgeschichte, in drei Gruppen aufgeteilt. Die Karzinome sind mit 80 Prozent Anteil die größte Gruppe unter den Tumoren. Sie entstehen im Deckgewebe der Haut, in der Schleimhaut und im Drüsengewebe. Sarkome wachsen in Fettgewebe, Sehnen, Muskeln, Knochen oder Knorpel. Blastome sind Tumoren, die bei der Entwicklung des Gewebes und der Organe enstehen. Neben bösartigen oder malignen Tumoren gibt es auch gutartige (benigne) Krebsgeschwulste. 
@iStock / DStarky
Die häufigsten Krebsarten bei Männern (Neuerkrankungen pro Jahr):
1. Prostatakrebs 65.200 (10-Jahrestendenz: + 2,8 %)
2. Lungenkrebs 35.290 (+ 3,9 %)
3. Darmkrebs 33.920 (– 4 %)
4. Harnblasenkrebs 13.500 (+ 4,8 %)
5. Malignes Melanom der Haut 12.010 (+ 34,8 %)
6. Non-Hodgkin-Lymphome 10.190 (+ 40,2 %)
7. Pankreaskrebs 9.860 (+ 33,4 %)
8. Krebs von Mundhöhle und Rachen 9.820 (+ 3,2 %)
9. Nierenkrebs 9.350 (+ 4,4 %)
10. Magenkrebs 9.200 (– 0,1 %)
11. Leukämien 6.870 (+ 8,4 %)
12. Speiseröhrenkrebs 5.710 (+ 19 %)
13. Hodenkrebs 4.160 (+ 4,8 %)
14. Kehlkopfkrebs 2.770 (– 23,3 %)
15. Schilddrüsenkrebs 1.930 (+ 12,9 %)
Die häufigsten Krebsarten bei Frauen (Neuerkrankungen pro Jahr):
1. Brustkrebs 69.900 (10-Jahrestendenz: – 2,5 %)
2. Darmkrebs 25.710 (– 14,4 %)
3. Lungenkrebs 21.930 (+ 40,8 %)
4. Malignes Melanom der Haut 10.880 (+ 22,4 %)
5. Gebärmutterkörperkrebs 10.860 (– 3,7 %)
6. Pankreaskrebs 9.160 (+ 21 %)
7. Non-Hodgkin-Lymphome 8.280 (+ 28,8 %)
8. Eierstock- und Eileiterkrebs 7.300 (– 6,3 %)
9. Magenkrebs 5.560 (– 16,5 %)
10. Nierenkrebs 5.480 (– 1,1 %)
11. Leukämien 5.310 (+ 4,5 %)
12. Harnblasenkrebs 4.770 (+ 5,8 %)
13. Krebs von Mundhöhle und Rachen 4.490 (+ 28,7 %)
14. Gebärmutterhalskrebs 4.320 (– 11,5 %)
15. Schilddrüsenkrebs 4.270 (+ 2,6 %) 
@iStock / SciePro
Krebs kann an vielen Stellen im menschlichen Körper auftreten und dabei völlig unterschiedliche Symptome entwickeln. Einige – auch häufige Krebsarten wie zum Beispiel Pankreaskrebs – verursachen dagegen bis wenige Monate vor dem Tod überhaupt keine Krebs-Anzeichen. 
@iStock / Anchiy
Medizinisches Cannabis wird in der Krebsmedizin eingesetzt, um Nebenwirkungen einer Krebstherapie abzumildern. Zum Einsatz kommt medizinisches Cannabis in der Onkologie hauptsächlich als:
Antiemetikum u003e Verhindert Übelkeit und Erbrechen. Beides eine häufige Nebenwirkung bei Chemotherapien.
Appetitanreger u003e Das „Heißhunger-Hormon“ Ghrelin kann bei einer Chemotherapie unterdrückt werden. Dadurch wird das Hungergefühl unterdrückt. Die Wirkstoffe von medizinischem Cannabis sind in der Lage, direkt die entsprechenden Rezeptoren des Gehirns zu besetzen und sogar das Sättigungshormon Leptin fernzuhalten.
Durchfall-Stopper u003e Durchfall gehört zu den häufigsten Nebenwirkungen vieler Krebstherapien wie Chemo- und Strahlentherapie, kann aber auch ein Symptom verschiedener Krebsentitäten wie Lymphome, Darmkrebs und Pankreaskrebs sein. Medizinisches Cannabis hat in medizinischen Studien eine positive Wirkung auf den Verdauungstrakt gezeigt, denn im gesamten Verdauungstrakt gibt es viele Cannabinoid-Rezeptoren. Diese könnten durch THC und CBD aktiviert werden und entzündungshemmend wirken. Vor allem die CB1-Rezeptoren könnten eine wichtige Rolle spielen.
Antidepressivum u003e CBD-haltige Präparate haben einen stimmungsaufhellenden Effekt. Das kann Angstzuständen, Panikattacken oder anderen psychischen Belastungen gegensteuern. Die Laune des Betroffenen wird gehoben, Stress verringert und selbst die Schlafqualität verbessert. Aber: Auch wenn medizinisches Cannabis zwar kurzfristig die Stimmung aufhellen kann, muss das nicht von Dauer sein. Eine engmaschige ärztliche Begleitung ist deswegen unumgänglich.
Schmerzmittel u003e Krebs im finalen Stadium kann sehr starke Schmerzen verursachen. Hier kann Betroffenen mit starken Morphiumgaben gut geholfen werden. Weil Morphium aber sehr schnell abhängig macht, kann medizinisches Cannabis, das nicht abhängig macht, eine gute Alternative sein, wenn die Schmerzen noch nicht so stark sind.
Medizinisches Cannabis als Krebsmedikament u003e Bei der Therapie von Nebenwirkungen kann medizinisches Cannabis eine wichtige Rolle spielen. Medizinisches Cannabis als Krebs-Medikament, also als Arznei, die direkt bösartige Zellen angreift, ist nicht in Sicht. Es gibt auch keine wissenschaftlichen Belege für die Wirksamkeit. 
@iStock / greenleaf123
Klares Nein. Es existiert keine einzige belastbare Studie, die eine heilende Wirkung von medizinischem Cannabis bei Krebserkrankungen belegt. Die Forschungs-Aktivitäten zu dieser Frage sind allerdings auch nicht unbedingt ehrgeizig. Ein Ansatz ist zu untersuchen, ob medizinisches Cannabis durch Belegung verschiedener Rezeptoren ein Tumorwachstum stoppen könnte. 
@iStock / janiecbros
Medizinisches Cannabis wirkt gut belegbar gegen neuropathische Schmerzen. Das sind Schmerzen, die im Nervensystem selbst entstehen. Im Gegensatz dazu stehen nozizeptive Schmerzen, die vom Nervensystem „nur“ ans Gehirn weitergeleitet werden. Medizinisches Cannabis hat sich gut in der Behandlung von leichteren Schmerzen bewährt und kann deswegen auch unter ärztlicher Kontrolle bei durch Krebs verursachten Schmerzen eingesetzt werden. 
@iStock / Esther Kelleter
Dieser Artikel beinhaltet lediglich allgemeine Informationen zu einem Gesundheitsthema und dient somit nicht der Selbstdiagnose, -behandlung oder -medikation. Er ersetzt keinesfalls einen Arztbesuch. Individuelle Fragen zu Krankheitsbildern dürfen unsere Redakteure nicht beantworten.
Bildquelle Titelbild: ©iStock.com / Mohammed Haneefa Nizamudeen
Disclaimer
Die Inhalte der mediorbis-Artikel werden mit größtmöglicher Sorgfalt recherchiert und umgesetzt. Wir bemühen uns, die Informationen aktuell, inhaltlich korrekt und vollständig anzubieten. Dennoch ist das Auftreten etwaiger Fehler nicht auszuschließen. Eine Haftung für die Richtigkeit, Vollständigkeit und Aktualität kann daher trotz sorgfältiger Prüfung nicht übernommen werden. mediorbis übernimmt insbesondere keinerlei Haftung für eventuelle Schäden oder Konsequenzen, die durch die direkte oder indirekte Nutzung der angebotenen Inhalte entstehen. Hinweise und Korrekturen nehmen wir gerne entgegen; mailen Sie an mrb@mediorbis.de.